Magnesium, Mg
Fazit:
Eine naturnahe und ausgewogene vegane Ernährung deckt den Bedarf an Magnesium besser ab als Mischkost.
Vorkommen:
Gute Magnesium-Lieferanten sind Samen und Nüsse wie Hanfsamen (700 mg/100g), Leinsamen (390), Sesam (351), Sonnenblumenkerne (325), Cashew (290), Mandeln (270) und Haselnüsse (163). Aber auch in Vollkorngetreide, Hülsenfrüchten und grünem Gemüse wie Buchweizen (230), Quinoa (197), Mungobohne (190), Spinat (79) und Mangold (81) sind gute Mengen Magnesium enthalten.3
Lager- und Zubereitungsverluste:
Magnesium gelangt beim Kochen ins Kochwasser, deshalb sollte man möglichst kurz dämpfen und das Kochwasser nicht wegleeren.
Ernährung / Gesundheit:
Magnesium (Mg) gehört zu den essentiellen Mengenelementen und ist eines der zehn häufigsten Elemente der Erde. Essentiell bedeutet, dass unser Körper den Stoff nicht selbst herstellen (synthetisieren) kann, ihn aber in gewissen Mengen benötigt. Im Blattgrün der Pflanzen, dem Chlorophyll, ist Magnesium zu etwa 2 % enthalten.
Tagesbedarf auf lange Sicht:
Die Zufuhr-Empfehlungen (D-A-CH-Referenzwerte) für eine tägliche Magnesiumzufuhr liegen für Frauen je nach Alter zwischen 300 und 350 mg/Tag und für Männer zwischen 350 und 400 mg/Tag. Während der Stillzeit ist der Bedarf erhöht und liegt bei 390 mg/Tag.
Mangelsymptome:
Schwere Mangelzustände treten bei Nierenfunktionsstörungen, langandauerndem Durchfall, chronischen Darmentzündungen, schlecht eingestelltem Diabetes mellitus, Kortikoiden, bestimmten Diuretika oder Alkoholismus mit Fehlernährung auf.
Überversorgung:
Zu einer Hypermagnesiämie (Magnesiumüberschuss) kommt es überwiegend bei verminderter renaler Ausscheidung, endokrinen Erkrankungen, erhöhter Magnesium-Zufuhr oder endogener Magnesiumfreisetzung. Bei Überdosierung von Magnesium (in Form von Salzen) kann es zu osmotisch bedingten Durchfällen kommen.
Funktionen im Körper etc.:
Magnesium ist essentieller Cofaktor von über 300 enzymatischen Reaktionen des Intermediärstoffwechsels, vor allem bei ATP- und Nukleinsäure-bindenden Enzymen.
Magnesium ist Bestandteil folgender intra- und extrazellulärer Prozesse:1,2,4
- Neuromuskuläre Erregungsleitung und -weiterleitung sowie Muskelkontraktion (physiologischer Calcium-Antagonist)
- Stabilisierung biologischer Membranen und Beeinflussung der Zelladhäsion
- Thrombozytenaggregation
- Modulation von Ionenpumpen beziehungsweise -kanälen (z.B. Kaliumkanäle in den Herzmuskelzellen)
- Energiegewinnung und -bereitstellung
- Speicherung und Freisetzung von Hormonen und Neurotransmittern. Magnesium hemmt sowohl die Funktion des Parathormons als auch die Freisetzung von Adrenalin und Noradrenalin. Mit sinkendem Magnesium-Serumspiegel steigt infolge der erhöhten Ausschüttung der Stresshormone Adrenalin und Noradrenalin die Empfindlichkeit gegenüber Stress.
- Mineralisation und Wachstum der Knochen.
Aufnahme und Stoffwechsel:
Die Magnesiumresorption findet im oberen Dünndarm statt, aber auch im übrigen Verdauungstrakt. Unter normalen Bedingungen beträgt die Absorptionsrate zwischen 35 und 55 %. Die Resorption erfolgt sowohl durch passive Diffusion als auch durch einen Carrier-vermittelten Prozess. Bei einem hohen Angebot an Magnesium ist dieser Transportmechanismus gesättigt und die resorbierte Magnesiummenge nimmt prozentual ab. Umgekehrt resultiert aus einer geringen Magnesiumzufuhr oder einem Magnesiummangelzustand ein Anstieg der intestinalen Resorption.1
Die Absorption bzw. Bioverfügbarkeit des Mineralstoffs hängt von zahlreichen Faktoren ab, wie der Zusammensetzung der Nahrung, Interaktion mit anderen Elementen, Flüssigkeitsaufnahme und Lebensalter.
Speicherung, Verbrauch, Verluste:
Der Körper eines Erwachsenen enthält etwa 20 g Magnesium. Etwa 95 % des gesamten Magnesiumbestandes im Körper befindet sich in den Körperzellen. Davon sind 50-70 % in gebundener Form als Hydroxylapatit in den Knochen lokalisiert. Ca. 28 % des intrazellulär vorhandenen Magnesiums sind in der Muskulatur und der restliche Anteil im Weichteilgewebe gespeichert.
Nur das ionisierte beziehungsweise freie Magnesium ist biologisch aktiv.
Der Körper hält die freie extrazelluläre Magnesiumkonzentration durch Anpassung von Resorption, Ausscheidung und Austausch mit den Speichern im Skelett mit Hilfe eines komplexen hormonellen Regelsystems in einem sehr engen Bereich konstant. Parathormon und "Calcitri.." (metabolisch aktive Form von Vitamin D) stimulieren die Magnesiumrückresorption und hemmen die renale (über die Nieren) Magnesiumausscheidung.
Ein Magnesiumüberschuss veranlasst die Schilddrüse, vermehrt Calcitonin zu synthetisieren und frei zu setzen. Calcitonin, ein Peptidhormon, stimuliert die renale Magnesiumausscheidung und senkt damit die extrazelluläre Magnesiumkonzentration. Calcitonin stellt einen direkten Antagonisten zum Parathormon dar. Neben Calcitonin können weitere Hormone und eine hohe Zufuhr von Calcium die renale Rückabsorption von Magnesium herabsetzten.1,2,4,5
Die Nieren resorbieren bis 97 % zurück, dadurch steht Magnesium dem Organismus erneut zur Verfügung.
Strukturen:
Da Magnesium eine grosse chemische Reaktionsfähigkeit aufweist, kommt es in der Natur nicht in elementarer, sondern ausschliesslich in kationisch gebundener Form vor – beispielsweise als Magnesit (MgCO3), Dolomit (MgCO3*Ca-CO3) oder Magnesiumchlorid (MgCl2).
Literatur / Quellen:
- Biesalski HK, Fürst P, Kasper H, Kluthe R, Pölert W, Puchstein Ch, Stähelin HB: Ernährungsmedizin. 125-126, 167-169. Georg Thieme Verlag, Stuttgart 1999.
- Biesalski Hans Konrad und Grimm Peter: Taschenatlas der Ernährung; 6. Auflage (2015); Georg Thieme Verlag, Stuttgart und New York.
- US-Amerikanische Nährwertdatenbank USDA.
- Elmadfa Ibrahim und Leitzmann Claus: Ernährung des Menschen; 5. Auflage (2015); Verlag Eugen Ulmer, Stuttgart.
- Elmadfa Ibrahim und Meyer Alexa: Ernährungslehre, 3. Auflage (2015); Verlag Eugen Ulmer, Stuttgart.
- De Groot Hilka und Farhadi Jutta: Ernährungswissenschaft; 6. Auflage (2015); Verlag Europa-Lehrmittel, Haan-Gruiten.
Dieser Nudelsalat mit Artischocken, Bohnen, Kirschtomaten und Vollkorn-Teigwaren sättigt gut und lässt sich einfach zubereiten.
Für diese weisse Bohnen mit Apfel, Birne und Bratkartoffeln weicht man davor Bohnen über Nacht in Wasser ein. Im Buch findet sich ein passender Löwenzahnsalat.
Dieses Basisrezept für vegane Teriyaki-Spiesse mit Sonnenblumenkernen und Lauch lässt sich schön mit Gemüse kombinieren. Alternative zu deftigen Grillspiessen.
Agar-Agar, meist aus Rotalgen (Seetang), ist ein pflanzliches Geliermittel und ist auch in Forschung/Medizin im Einsatz. Es ist bio erhältlich, aber nie roh.
Rotalgenblätter (Nori-Blatt, bio?) für Sushi sind leicht geröstet, also nicht roh im Gegensatz zu unbehandelten Rotalgenblättern bzw. Nori-Blättern.
Getrocknetes Basilikum (bio) ist ein wichtiges Gewürz der mediterranen Küche und passt gut zu Rohkost, Salat, Tomaten, Marinaden etc. Auch roh erhältlich.






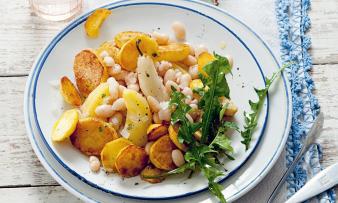




Kommentare