Cómo una dieta basada en plantas puede prevenir la diabetes
Para 2024, una de cada nueve personas en todo el mundo padecía diabetes. La cifra aumenta cada año. Una dieta basada en plantas puede prevenirla o reducir el ri
Tabla de contenido
- ¿Qué es la diabetes?
- ¿Por qué las personas desarrollan diabetes tipo 2?
- Medidas nutricionales para la prevención y el control (remisión)
- ¿Prefieres una dieta saludable basada en plantas?
- Evite los cereales refinados, las bebidas azucaradas y los dulces.
- Evitar o reducir los productos animales
- Reducir las grasas saturadas
- ¿Dieta alta en proteínas como terapia para la diabetes?
- ¿Consumo de alimentos “que reducen el azúcar en la sangre”?
- Frecuencia de las comidas
- Sobrepeso y obesidad
- Falta de ejercicio
- Contaminantes orgánicos persistentes (COP)
- Conclusión
- Bibliografía
¿Qué es la diabetes?
En la diabetes, los niveles de azúcar en sangre se mantienen elevados durante períodos prolongados. Esto ocurre porque el cuerpo no produce insulina o ya no puede utilizarla correctamente. Si esta afección persiste, provoca daños en los vasos sanguíneos, nervios y órganos. La diabetes no tratada puede provocar amputaciones y, finalmente, la muerte.
Los humanos ingerimos carbohidratos a través de los alimentos. El sistema digestivo los descompone en azúcares simples específicos, según su tipo. El almidón produce principalmente glucosa, el azúcar de mesa (sacarosa) produce glucosa y fructosa, y el azúcar de la leche (lactosa) produce glucosa y galactosa. Tras su absorción en el intestino, los tres azúcares viajan a través de la vena porta hasta el hígado. Si bien el metabolismo de la fructosa y la galactosa ocurre principalmente en el hígado, este solo absorbe una parte de la glucosa (y la convierte en glucógeno). El resto ingresa al torrente sanguíneo, elevando así los niveles de azúcar en sangre.
La hormona insulina, producida por el páncreas, asegura que la glucosa de la sangre entre en las células (principalmente las musculares y las adiposas), donde sirve como fuente de energía. La insulina actúa como una llave que abre las puertas celulares, permitiendo que la glucosa entre en ellas. De esta manera, la insulina regula los niveles de azúcar en sangre.
En la diabetes, el mecanismo de captación de glucosa se ve afectado. Como resultado, los niveles de azúcar en sangre permanecen elevados. Esto puede tener dos causas:
- El cuerpo produce poca o ninguna insulina en el páncreas (falta la "clave").
- Las células ya no responden suficientemente a la insulina, se produce la llamada resistencia a la insulina (la "cerradura" está rota, por lo tanto la "llave" ya no funciona correctamente).
Debido a estos dos trastornos se distinguen oficialmente dos formas de diabetes:
| forma | Posibles causas | Características | Tratamiento |
| Diabetes tipo 1: deficiencia de insulina |
|
| inyecciones de insulina |
| Diabetes tipo 2: Resistencia a la insulina
|
|
| Es posible que sean necesarios ajustes en la dieta y el estilo de vida, medicación y posiblemente inyecciones de insulina a largo plazo. |
Información sobre la diabetes tipo 1
La diabetes mellitus tipo 1 (DM1) es una enfermedad autoinmune crónica. En esta enfermedad, el sistema inmunitario destruye por error las células beta productoras de insulina en el páncreas. Esto provoca una deficiencia absoluta de insulina. Aproximadamente entre el 5 % y el 10 % de los casos de diabetes son de DM1, y la enfermedad suele manifestarse en la infancia, la adolescencia o la adultez temprana. Clínicamente, la DM1 solo se manifiesta cuando se ha perdido entre el 80 % y el 90 % de la masa de células beta. Esto requiere tratamiento con insulina de por vida. Sin embargo, el proceso autoinmune suele comenzar años antes de los primeros síntomas: durante esta fase, se forman autoanticuerpos contra antígenos de las células de los islotes, como la insulina, el GAD o el IA-2. Además, la inmunidad celular desempeña un papel fundamental, en particular los linfocitos T y las citocinas inflamatorias, que dañan gradualmente las células beta.4
La enfermedad surge de una interacción entre la predisposición genética y factores ambientales. La asociación genética con los alelos HLA de clase II es particularmente fuerte.4 Sin embargo, otros factores ambientales son necesarios para la aparición de la enfermedad. Entre estos, las infecciones virales se consideran desencadenantes particularmente relevantes, respaldados por hallazgos epidemiológicos y experimentales. Los patrones estacionales y geográficos en la incidencia de la diabetes mellitus tipo 1 (DM1) respaldan esta suposición. Los virus sospechosos incluyen enterovirus (especialmente Coxsackie B4), virus de la parotiditis y la rubéola, citomegalovirus (CMV), rotavirus, virus de la influenza y SARS-CoV-2.4
Los enfoques de investigación alternativos enfatizan cada vez más que la diabetes tipo 1 no debe entenderse únicamente como una enfermedad autoinmune clásica. Más bien, es el resultado de una interacción errónea entre el estrés de las células beta y el sistema inmunitario. Roep et al. (2021) argumentan que, debido a su alta carga metabólica, su marcada susceptibilidad al estrés y sus limitados mecanismos de protección, las células beta contribuyen activamente a su propio reconocimiento inmunitario. En condiciones inflamatorias, alteran su presentación antigénica, liberan quimiocinas como CXCL10 y generan nuevos péptidos inmunogénicos mediante procesos de estrés. Estas señales atraen y activan las células inmunitarias, de modo que la reacción autoinmunitaria no surge principalmente de células T "mal dirigidas", sino de células beta alteradas que provocan una respuesta inmunitaria. Este enfoque amplía la comprensión tradicional de la diabetes tipo 1 y subraya la necesidad de estrategias terapéuticas dirigidas tanto al sistema inmunitario como a la salud de las células beta.5
Estudios epidemiológicos tempranos mostraron una correlación moderadamente alta entre la exposición muy temprana a la leche de vaca en la infancia y la aparición de diabetes tipo 1.6 Estudios más recientes presentan un panorama heterogéneo. Algunos estudios continúan identificando asociaciones, mientras que otros no encuentran ningún efecto. Un problema radica en que numerosos factores de confusión, como la corta duración de la lactancia materna, las infecciones o la predisposición genética, son difíciles de distinguir del efecto potencialmente negativo de la leche de vaca. Por lo tanto, la investigación actual se está alejando de la idea de un desencadenante directo y considera la leche de vaca más como un posible modulador ("desencadenante") dentro de una compleja interacción entre la barrera intestinal, el sistema inmunitario, las infecciones y la susceptibilidad genética.7,8,9
Los síntomas graves aparecen en pocos días o semanas. Estos pueden incluir sed intensa, pérdida de peso inexplicable, fatiga, dolor abdominal, náuseas y aliento dulzón (en casos de cetoacidosis). Además de medir la glucemia, también se realiza una prueba de autoanticuerpos. La medición del nivel de péptido C también indica la cantidad de insulina que aún se produce en el cuerpo.
Otras formas de diabetes
Oficialmente existen dos formas de diabetes.
Extraoficialmente, la diabetes tipo 3 abarca varios subtipos de diabetes. Estos pueden ser causados por enfermedades pancreáticas (tumores, lesiones), trastornos hormonales o por medicamentos o sustancias químicas. En ocasiones, también se incluye la diabetes de inicio en la madurez (MODY, por sus siglas en inglés). Esta es una forma monogénica de diabetes, genéticamente determinada.
La diabetes tipo 4 se utiliza a veces como término para la diabetes gestacional. Se refiere a la diabetes que aparece por primera vez durante el embarazo. Suele desaparecer después del parto, pero aumenta el riesgo de desarrollar diabetes más adelante. En artículos de divulgación científica también se utiliza el término para la "diabetes del adulto" (tipo 2) en mujeres con peso normal.
Una forma particular de diabetes en personas con peso normal o bajo es la diabetes tipo 5. Su nombre en inglés es diabetes mellitus asociada a la desnutrición (UADM). Esta se presenta predominantemente en países en desarrollo y emergentes, generalmente en personas que experimentaron desnutrición grave o crónica durante la infancia o la adolescencia.60,61
¿Por qué las personas desarrollan diabetes tipo 2?
En la diabetes tipo 2, el metabolismo de la glucosa se altera. Esto se debe a que las células del cuerpo ya no responden adecuadamente a la insulina (resistencia a la insulina). Inicialmente, el cuerpo intenta compensar este efecto haciendo que el páncreas libere más insulina. Sin embargo, con el tiempo, esta sobreproducción constante sobrecarga las células beta, lo que provoca una disminución de su eficiencia. La producción de insulina disminuye. Esto significa que el cuerpo no puede utilizar la insulina (resistencia a la insulina) ni producir suficiente. Esto último se denomina "deficiencia relativa de insulina". Dado que el páncreas aún conserva la capacidad fundamental de producir insulina, la cantidad ya no es suficiente. Sin intervención, los niveles de glucosa en sangre permanecen elevados de forma permanente. Los músculos, el hígado y el tejido adiposo se ven afectados principalmente.
La diabetes tipo 2 suele desarrollarse gradualmente. La etapa precursora (prediabetes) suele pasar desapercibida durante años. Los niveles de azúcar en sangre se mantienen elevados de forma persistente, pero aún por debajo del umbral oficial de diabetes. Esta etapa inicial no se considera una enfermedad. Los términos típicos para describirla son "alteración de la tolerancia a la glucosa" o "niveles anormales de azúcar en sangre en ayunas". Sin embargo, los estudios demuestran que incluso las personas con prediabetes pueden sufrir daño orgánico. Además, el riesgo de desarrollar diabetes tipo 2 es muy alto.
La diabetes tipo 2, como enfermedad, no se hereda directamente; sin embargo, la predisposición genética y epigenética sí lo es. Esta predisposición hereditaria, combinada con otros factores de riesgo, aumenta la probabilidad de desarrollar la enfermedad.10
- Sobrepeso / Obesidad (Adiposidad) / IMC alto48,49
- Dieta alta en grasas y calorías (productos altamente procesados, incluyendo alto contenido de azúcar) y alta proporción de productos animales 13,25,26
- Falta de ejercicio66
- Contaminantes orgánicos de los alimentos y el medio ambiente69, 70, 71
- diabetes gestacional previa
- Condiciones preexistentes: síndrome de ovario poliquístico (SOP), presión arterial alta y enfermedad cardiovascular
- estrés crónico91
- sueño irregular92
- Fumar93
Los desencadenantes de la resistencia a la insulina incluyen los siguientes cambios metabólicos:
- El exceso de grasa corporal, especialmente en la cavidad abdominal profunda (grasa visceral), libera sustancias proinflamatorias. La inflamación crónica en el cuerpo altera la función de los receptores de insulina. Esto altera las vías de señalización a través de las cuales la insulina transporta normalmente el azúcar a las células.49
- La falta de ejercicio hace que las células musculares absorban menos glucosa y sean menos sensibles a la insulina.66
La nutrición es el factor decisivo: moldea los hábitos alimenticios e influye en el peso. Además, determina la cantidad de contaminantes orgánicos tóxicos que ingresan al organismo.
La diabetes tipo 2 se puede prevenir. Médicamente, se considera una enfermedad crónica y no se puede curar en el sentido tradicional. Sin embargo, los estudios demuestran que la remisión (control) es posible mediante la pérdida de peso, cambios en la dieta y ejercicio . Los niveles de azúcar en sangre se mantienen normales de forma permanente. Si estas medidas no son suficientes para normalizar los niveles de azúcar en sangre, se utilizan medicamentos. A largo plazo, pueden ser necesarias inyecciones de insulina si las células beta pierden su capacidad de producir insulina debido a la sobreproducción persistente de insulina para compensar la resistencia a la insulina.
Síntomas y resultados de pruebas para la diabetes tipo 2
El cuerpo puede compensar los niveles elevados de azúcar en sangre durante mucho tiempo. Por eso, muchas personas se sienten inicialmente perfectamente sanas. Los síntomas solo aparecen cuando los niveles aumentan significativamente.
A diferencia de la diabetes tipo 1, los análisis de sangre regulares juegan un papel central en la detección temprana de la diabetes tipo 2. Incluso en las primeras etapas (prediabetes), los niveles elevados de azúcar en sangre se pueden detectar a través de pruebas como la glucemia en ayunas, la glucemia a largo plazo (valor HbA1c) o la prueba de tolerancia a la glucosa oral.
Como medida preventiva, se recomienda controlar periódicamente los niveles de azúcar en sangre (aproximadamente cada 3 años) a partir de los 35 años. Las personas con factores de riesgo deben hacerse la prueba antes.
Límites de azúcar en sangre según Diabetes Suiza: 3
azúcar en sangre en ayunas
La glucemia en ayunas mide el nivel de glucosa en sangre en un momento específico. Revela fluctuaciones agudas, hipoglucemia o hiperglucemia. Es útil para el seguimiento de la terapia en la vida diaria.
- Rango normal: < 100 mg/dl (< 5,6 mmol/l)
- Prediabetes: 100-125 mg/dL (5,6-6,9 mmol/L)
- Diabetes mellitus: ≥ 126 mg/dl (≥ 7,0 mmol/l)
Valor de HbA1c ("azúcar en sangre a largo plazo")
El valor de HbA1c (glucemia a largo plazo) indica el nivel promedio de glucosa en sangre durante las últimas 8 a 12 semanas. Se considera una herramienta importante para el diagnóstico y el seguimiento de la diabetes.
- Diabetes mellitus: ≥ 6,5 % (≥ 48 mmol/mol)
- Prediabetes: 5,7% - 6,4% (39-47 mmol/mol)
- Normal: < 5,6% (aprox. 20-38 mmol/mol)
El valor óptimo de HbA1c para un adulto sano y no diabético se encuentra en el límite inferior del rango normal, aproximadamente entre el 4,8 % y el 5,2 %. Un valor de HbA1c inferior al 4 % es poco frecuente y puede indicar trastornos de los glóbulos rojos.
Medidas nutricionales para la prevención y el control (remisión)
Para las personas diagnosticadas con diabetes tipo 2, la nutrición es uno de los mayores desafíos. Dada la importancia de la dieta, es crucial que quienes la padecen participen directamente en el desarrollo de su plan de tratamiento, busquen información activamente y se eduquen sobre el tema. A continuación, ofrecemos consejos importantes sobre qué considerar para prevenir o controlar (remisión) la diabetes.
¿Prefieres una dieta saludable basada en plantas?
El ensayo clínico aleatorizado de Kahleova et al. (2011) investigó los efectos de una dieta vegetariana baja en calorías en comparación con una dieta convencional para diabéticos en personas con diabetes tipo 2 (24 semanas). El 43 % del grupo vegetariano logró reducir su medicación, en comparación con solo el 5 % del grupo control. El grupo vegetariano experimentó una mayor pérdida de peso y redujo significativamente su grasa visceral. La sensibilidad a la insulina mejoró un 10 % más que con la dieta convencional.11 El grupo vegetariano también experimentó menos atracones, menos hambre y mejor estado de ánimo.12
Esto lo confirma un estudio aleatorizado de Hanick et al. (2025). Una dieta integral basada en plantas, combinada con ejercicio moderado, resulta en un control significativamente mejor de la glucemia y una reducción del uso de medicamentos en personas con diabetes tipo 2 (el 63 % logró reducir su medicación). La remisión de la enfermedad se produjo en el 23 % de los participantes con HbA1c < 9 %. Además, los marcadores cardiovasculares también mejoraron.81 Se observa un efecto positivo en la HbA1c y el peso con las dietas vegetarianas y veganas, como lo confirma la revisión sistemática de Lv et al. (2025). Sin embargo, una dieta vegana produjo mejores parámetros cardiovasculares que una dieta lactovegetariana.82
Los siguientes hábitos alimentarios son cruciales para el desarrollo o la prevención de la diabetes tipo 2:13,17
| Alimentos que favorecen la diabetes tipo 2 | Alimentos que previenen/reducen la diabetes tipo 2 |
| Alto consumo de:
| Alto consumo de:
|
Coma alimentos antiinflamatorios de origen vegetal
La inflamación es una reacción natural del cuerpo humano para combatir infecciones y curar lesiones. Los alimentos vegetales contienen fitoquímicos, que tienen un efecto antioxidante.
Los carotenoides, una clase de compuestos vegetales presentes en frutas y verduras rojas, amarillas y anaranjadas, tienen propiedades antiinflamatorias comprobadas. Numerosos estudios demuestran que cuanto mayor sea la concentración de carotenoides en el cuerpo humano, menor será el riesgo de desarrollar diabetes.10
 | El propósito de la inflamación es reparar el tejido dañado. Normalmente, esta es una respuesta a corto plazo. El estrés oxidativo y un desequilibrio en el sistema inmunitario pueden provocar que la inflamación se vuelva crónica. El contacto del sistema inmunitario con un factor externo (un patógeno o un alimento) desencadena la liberación de citocinas proinflamatorias. Estas citocinas pueden aumentar directamente la resistencia a la insulina en las células musculares y hepáticas.14 |
Consuma más legumbres
Una revisión sistemática de 41 ensayos controlados aleatorizados (ECA) confirma que el consumo regular de legumbres mejora de forma demostrable el control de la glucemia. En los estudios evaluados, las legumbres por sí solas redujeron los niveles de glucemia e insulina en ayunas. Al incorporarlas a una dieta de bajo índice glucémico o rica en fibra, también mejoran la HbA1c. Sin embargo, la magnitud de estos efectos varía considerablemente entre estudios.15
Numerosos estudios confirman el efecto reductor del azúcar en sangre y del colesterol de las habas (Vicia faba) y los frijoles mungo (así como del fenogreco).16
Un mayor consumo de legumbres ( frijoles, garbanzos, lentejas ) se asocia con una ligera reducción del riesgo de diabetes tipo 2 en la mayoría de los estudios de cohorte a gran escala. Sin embargo, los resultados son heterogéneos.90
La pequeña reducción del riesgo puede deberse a la forma en que se preparan las legumbres. Platos populares como los guisos de frijoles con carne, los frijoles en salsa de tomate azucarada o las lentejas con leche de coco anulan el efecto positivo. Por lo tanto, conviene combinar legumbres con verduras y evitar añadir alimentos azucarados o grasosos.
| Esto no es sólo para veganos o vegetarianos: Los veganos suelen comer de forma poco saludable. Errores nutricionales evitables . |
Evite los cereales refinados, las bebidas azucaradas y los dulces.
Los carbohidratos son importantes fuentes de energía. En particular, los carbohidratos de cadena corta (p. ej., azúcares simples como la glucosa y disacáridos como la sacarosa) se absorben rápidamente y tienen un impacto significativo en los niveles de azúcar en sangre. El cuerpo utiliza los azúcares simples directamente; no se descomponen.
Los carbohidratos de rápida digestión se encuentran en dulces, jugos de fruta, bebidas azucaradas y postres (pasteles, chocolate, etc.). Los productos bajos en fibra (productos de granos refinados, productos de papa) también provocan un aumento rápido de la glucemia.
Los carbohidratos complejos (carbohidratos de cadena larga) tienen un mayor contenido de fibra y, por lo tanto, tienen un efecto débil sobre la glucemia. Entre ellos se encuentran las verduras con almidón, ciertas frutas, el arroz integral y los cereales integrales (y sus derivados). Las legumbres, los frutos secos, las semillas, las verduras sin almidón y los pseudocereales también contienen carbohidratos.
Un 2016 Un estudio publicado con más de 200.000 personas sobre la relación entre los hábitos alimentarios y el estado de salud concluyó que el riesgo de desarrollar diabetes tipo 2 puede aumentar incluso con una dieta poco saludable basada en plantas. En cambio, el consumo de cereales integrales se asocia con un riesgo significativamente menor de desarrollar diabetes tipo 2.17
Según los investigadores, los siguientes elementos de una dieta poco saludable basada en plantas pueden aumentar el riesgo de diabetes:
| Elementos de una dieta poco saludable basada en plantas | |
| Jugos de frutas | Sidra de manzana (sin alcohol) o jugo de manzana, jugo de naranja, jugo de pomelo, todos los demás jugos de frutas |
| Grano refinado | Cereales para el desayuno elaborados con granos refinados, pan blanco, panecillos con levadura y otros, bagels, muffins, galletas, arroz blanco, panqueques, waffles, galletas saladas, pastas (fideos). |
| papas | Papas fritas, papas al horno, puré de papas |
| bebidas azucaradas | Cola con cafeína y sin cafeína con azúcar, otras bebidas carbonatadas con azúcar, bebidas de frutas azucaradas sin gas |
| Dulces y postres | Chocolate, barras dulces con y sin chocolate, galletas caseras y compradas, brownies, donuts, pasteles, panecillos dulces de levadura, tartas, mermeladas, pudines, sémola de maíz, almíbar, miel. |
Las bebidas alcohólicas causan fluctuaciones en los niveles de azúcar en sangre. El alcohol puede provocar hipoglucemia grave (niveles bajos de azúcar en sangre) con efectos retardados. El hígado se encarga principalmente de descomponer el alcohol y no puede liberar glucosa al torrente sanguíneo. Las bebidas alcohólicas azucaradas, así como la cerveza de malta sin alcohol, elevan significativamente los niveles de azúcar en sangre. El consumo crónico de alcohol causa resistencia a la insulina y un deterioro de la función de las células beta pancreáticas, condiciones previas para el desarrollo de la diabetes.
Existen estudios sobre el alcohol y la diabetes que clasifican el consumo diario moderado como no perjudicial para la salud de las personas con diabetes mellitus. Sin embargo, según la OMS, no existe una cantidad de alcohol tolerable ni segura. Cualquier cantidad (etanol) daña el organismo y supera cualquier posible efecto positivo. Está clasificado como un potente carcinógeno.96
Un mayor consumo de carbohidratos complejos mejora el metabolismo del azúcar y, a menudo, contribuye a la pérdida de peso. Además, contienen valiosos nutrientes y fibra, que influyen positivamente en la saciedad y la digestión.
Métodos de cálculo y criterios de evaluación
Para ayudarle a mantener su nivel de azúcar en sangre bajo control, existen métodos simplificados diseñados para facilitar el manejo de alimentos ricos en carbohidratos. Estos sirven como herramientas, pero no reemplazan el conocimiento sobre una dieta saludable. Los cálculos precisos son especialmente importantes para las personas con diabetes tipo 1, ya que necesitan el contenido exacto de carbohidratos para determinar su dosis de insulina. Sin embargo, este conocimiento también ayuda a las personas con diabetes tipo 2 a evitar picos de azúcar en sangre. Tenga en cuenta que el contenido de carbohidratos de los alimentos naturales puede variar.
Unidades de pan (UB)
En los países de habla alemana, los carbohidratos todavía se calculan a veces con unidades de pan (BE). Una unidad de pan (1 BE) contiene 12 g de carbohidratos que afectan los niveles de azúcar en sangre. Desde 2010, no existen alimentos especiales para diabéticos, lo que también significa que los alimentos ya no se etiquetan con unidades de pan (BE).
Unidades de carbohidratos (CU)
Para calcular el contenido de carbohidratos de los alimentos, se utilizan unidades de carbohidratos. 1 KE corresponde a 10 g de carbohidratos. Este cálculo es más sencillo para el uso diario que usar unidades de pan, especialmente si se dispone de una tabla de información nutricional pero no de una báscula.
Tablas de información nutricional
Casi todos los alimentos envasados incluyen la clásica tabla de información nutricional, que indica el contenido de carbohidratos por cada 100 g. Esto es especialmente útil para alimentos precocinados y otros productos procesados. Preste siempre atención al tamaño de la porción. Para productos frescos (frutas y verduras), puede consultar el contenido de carbohidratos en bases de datos nutricionales en línea. Para ello, deberá pesar el alimento para calcular el valor.
Las tablas de intercambio de carbohidratos, bases de datos y aplicaciones facilitan la estimación de las cantidades de carbohidratos por porción.
Índice glucémico (IG) y carga glucémica (CG)
El índice glucémico (IG) no calcula los carbohidratos en sí, sino que es una medida cualitativa de la rapidez con la que un alimento que contiene carbohidratos eleva el nivel de azúcar en sangre. La escala va de 0 a 100, siendo la glucosa (dextrosa) 100. Un IG alto implica un aumento rápido del azúcar en sangre; un IG bajo, un aumento más lento.
Esto no calcula una dosis de insulina, pero el IG ayuda a estimar mejor su efecto. Esto facilita la selección de alimentos que favorecen la glucemia. Sin embargo, el IG solo se aplica a alimentos individuales, no a comidas completas.
La carga glucémica (CG) combina la cantidad consumida con la velocidad a la que aumenta el azúcar en sangre: (IG x carbohidratos en g/porción) / 100. Por ejemplo: una sandía tiene un IG alto de 70-80, pero la CG es de alrededor de 5 porque una porción (aprox. 120 g) contiene muy pocos carbohidratos.
Para el uso diario, existen tablas con valores de IG y GL que pueden utilizarse como guía.
Con las comidas mixtas, la respuesta glucémica suele ser difícil de predecir. Los siguientes factores influyen en el aumento de la glucemia:
- La fibra dietética ralentiza la digestión, lo que da lugar a un aumento más lento del azúcar en sangre.
- Preparación: La pasta o el arroz tendrán un efecto diferente dependiendo de si se cocinan al dente o blandos.
- Los alimentos que contienen grasas y proteínas pueden retrasar el aumento del azúcar en sangre porque ralentizan el vaciamiento gástrico.
- La madurez de las frutas (por ejemplo los plátanos) puede aumentar el nivel de azúcar en sangre.
- El grado de procesamiento afecta la velocidad de absorción de carbohidratos, por ejemplo, avena arrollada (más lenta) versus copos instantáneos (más rápidos).
Evitar o reducir los productos animales
Una ingesta elevada de proteínas de origen animal se asocia directamente con un mayor riesgo de diabetes tipo 2.25,26 Un aumento de 20 g de proteína animal en la ingesta diaria de proteínas aumentó el riesgo de diabetes tipo 2 en un 7 %. En el caso de las proteínas vegetales, la mayoría de los estudios no muestran un impacto negativo en el riesgo de diabetes.27 Chen et al. (2020) lo demuestran claramente en un estudio epidemiológico de cohorte de 22 años (1993-2004). Las proteínas de la carne, el pescado y los productos lácteos contribuyeron a las asociaciones adversas entre la proteína animal total y el riesgo de prediabetes. La proteína vegetal total, así como las proteínas de legumbres, frutos secos, cereales, patatas o frutas y verduras, no produjeron efectos adversos.28
Carne, aves y huevos
En particular, el consumo de carnes procesadas (salchichas, tocino, salami, etc.) se asocia con un riesgo significativamente mayor de diabetes mellitus y enfermedad coronaria. Esto se debe a las grasas saturadas y a las sustancias que las acompañan, como el sodio y los conservantes (nitratos, nitritos y nitrosaminas).29 Además, contienen productos finales de glicación (AEG). Estos se forman en una reacción no enzimática entre azúcares y proteínas, lípidos y ácidos nucleicos (reacción de Maillard). Además de promover el estrés oxidativo, también promueven la inflamación, contribuyendo así a la diabetes y las enfermedades cardiovasculares.30
El hierro hemo también es problemático. Esta forma de hierro se encuentra predominantemente en la carne roja (res, cerdo, cordero), las aves y el pescado, o se añade artificialmente a las alternativas vegetales a la carne. Su efecto prooxidante promueve la formación de especies reactivas de oxígeno, que dañan las células y desencadenan inflamación. Su influencia en el metabolismo de aminoácidos y lípidos, junto con el aumento de las reservas de hierro, promueve el desarrollo de diabetes.31 También se asocia con un riesgo significativamente mayor de diabetes tipo 2. Un exceso de hierro hemo daña las células beta del páncreas, lo que afecta la secreción de insulina. No se ha demostrado tal asociación con el hierro no hemo.31,32,33
Los productos animales, como los huevos y la carne, contienen altos niveles de colina y L-carnitina. Cuando las bacterias intestinales descomponen la colina y la L-carnitina, se produce N-óxido de trimetilamina (TMAO). Esto promueve los procesos inflamatorios y se asocia con diversas enfermedades, como la aterosclerosis y la resistencia a la insulina.34
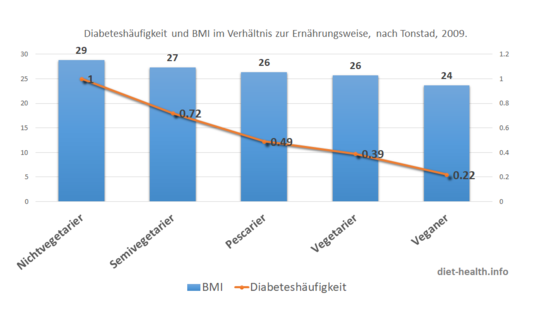
Un estudio de investigación sobre la prevalencia de diabetes tipo 2 en diferentes dietas, realizado en una población de más de 50.000 personas, mostró que el grupo no vegetariano presentó la tasa más alta de diabetes, así como los valores más altos de IMC.22 El estudio EPIC-Panacea, uno de los más completos sobre la relación entre el consumo de carne y el peso corporal, demostró que, en promedio, de dos personas con la misma ingesta calórica, la que consume más carne aumenta significativamente más de peso. Esto se logró mediante el seguimiento del aumento del IMC (índice de masa corporal) durante un período de 14 años. La carne roja, la carne procesada y las aves, en particular, se correlacionaron con un fuerte aumento de peso.23
Un estudio de 2010 realizado por la Universidad de Loma Linda (Departamento de Nutrición) confirma que eliminar la carne de la dieta es una forma eficaz de combatir la obesidad infantil.24
Leche y productos lácteos
Si la leche y los productos lácteos son adecuados para los diabéticos tipo 2 es un tema de debate controvertido.
La leche se considera un alimento con un índice glucémico (IG) bajo. Si bien la lactosa presente en la leche provoca un aumento de los niveles de azúcar en sangre, este aumento es significativamente menor que el de algunas frutas (como las manzanas y las naranjas). Sin embargo, a diferencia de las frutas, la leche no contiene fibra. La leche entera también contiene una alta proporción de grasas saturadas, que pueden promover la resistencia a la insulina y agravar la diabetes tipo 2.18,19
Excepción: ¿Yogur y productos lácteos bajos en grasa?
Un mayor consumo de productos lácteos, especialmente lácteos bajos en grasa, se asocia con un riesgo moderadamente menor de diabetes tipo 2 en mujeres en este amplio estudio a largo plazo.38 Otros estudios han arrojado resultados similares.39,40,41 Una revisión sistemática de 2019 concluyó que el yogur tuvo el efecto más fuerte.89 Aún no está claro si los productos lácteos en sí mismos son la razón del "efecto positivo" en estos estudios observacionales, o si otros factores del estilo de vida son responsables. Numerosas opciones de yogur vegano, como el yogur de soja, el yogur de avena o el yogur de almendras, también tienen un perfil de ácidos grasos más saludable.
En general, muchos científicos y autores consideran que los productos lácteos son alimentos no aptos para el ser humano.
Los productos lácteos son el alimento perfecto de la naturaleza, pero solo si eres un ternero. Hyman M. (2012) no recomienda la leche para personas con problemas de azúcar en la sangre.35
Desde una perspectiva evolutiva, el consumo regular de leche comenzó hace apenas 10.000 años con la domesticación del ganado. En muchas partes del mundo, el cuerpo deja de producir la enzima lactasa tras el destete. Dado que la lactasa es necesaria para descomponer la lactosa, el azúcar de la leche, en glucosa y galactosa, esta deficiencia enzimática provoca intolerancia a la lactosa, un fenómeno común en todo el mundo. Al mismo tiempo, algunas personas presentan una reacción inmunológica a las proteínas de la leche y desarrollan alergia a la misma. Si bien ciertas poblaciones, por ejemplo, en el norte de Europa, han desarrollado adaptaciones genéticas que permiten la producción de lactasa de por vida, la leche sigue siendo un alimento difícil de digerir para gran parte de la población mundial (aproximadamente el 65%).73 Lea más sobre esto aquí y aquí.
Se cree que uno de los tipos de proteína presentes en la leche (A1-beta-caseína) es un desencadenante del desarrollo de diabetes tipo 1 en niños genéticamente predispuestos que beben leche de vaca.72
La leche estimula al páncreas a producir más insulina. Se ha demostrado que la respuesta de la insulina al consumo de leche es mayor de lo que podría explicarse únicamente por la respuesta de la glucosa.36 Esto se debe a la caseína y la proteína de suero que contiene.36 Esto produce una mejora a corto plazo del metabolismo.37
Las células beta del páncreas ya están en sobreproducción en casos de resistencia a la insulina. Una estimulación adicional es perjudicial a largo plazo y provoca un agotamiento más rápido.87 Puede encontrar una explicación detallada de este efecto más adelante, en la sección "Dieta alta en proteínas".
En el siguiente artículo se explica por qué deberías preferir alternativas de origen vegetal y evitar la leche: ¡Mejor evitar la leche!
Reducir las grasas saturadas
La grasa del torrente sanguíneo llega a las células musculares y se deposita allí. Forma productos de degradación tóxicos (radicales libres) que causan inflamación y disfunción mitocondrial. Este fenómeno se denomina lipotoxicidad. Estos procesos bloquean la señalización de la insulina y provocan una acumulación de azúcar en el torrente sanguíneo. El efecto de la grasa sobre la función de la insulina se ha demostrado mediante infusiones de grasa en el torrente sanguíneo. Estas infusiones provocaron un aumento significativo de la resistencia a la insulina y una disminución de la captación de glucosa.18,19
Por el contrario, la eliminación de grasa del torrente sanguíneo reduce la resistencia a la insulina.20 En muchos casos, la tecnología de resonancia magnética también puede demostrar el vínculo entre la resistencia a la insulina y la transferencia de grasa de la sangre a los músculos. 21
Los ácidos grasos saturados se encuentran principalmente en productos animales . En los alimentos vegetales, solo se encuentran en cantidades muy pequeñas, con la excepción del aceite de coco, la manteca de cacao y el aceite de palma.
El aceite de palma contiene grandes cantidades de ácido palmítico saturado. Muchos alimentos procesados también contienen ácido palmítico. Este aumenta la resistencia a la insulina y provoca un mayor almacenamiento de grasa en el hígado.83
Reemplace las grasas saturadas con grasas monoinsaturadas (MUFA). En comparación con las grasas saturadas, estas mejoran la sensibilidad a la insulina. Sin embargo, este efecto positivo solo se aprecia con un consumo moderado de grasas.84
La opción más saludable es evitar el uso de aceite por completo. Todos los aceites son alimentos concentrados que han pasado por varios procesos de procesamiento. En general, son preferibles los alimentos integrales y mínimamente procesados, como los frutos secos o las semillas. Si decide usar aceite, opte por el aceite de linaza y el aceite de colza prensado en frío para platos fríos, y por el aceite de colza refinado para cocinar al vapor y cocinar. Use con moderaciónaceite de girasol, cacahuete, avellana o cártamo debido a su alto contenido en ácidos grasos omega-6 . Evite el aceite de palma y el aceite de coco, ya que son ricos en ácidos grasos saturados.
¿Dieta alta en proteínas como terapia para la diabetes?
En los últimos años, se ha investigado si una dieta alta en proteínas es beneficiosa para las personas con diabetes. Esto surgió a raíz de los resultados de un experimento mecanicista de 1915, que descubrió que los niveles de azúcar en sangre apenas aumentaban tras consumir proteínas. Estudios con animales realizados en las décadas de 1970 y 1980 confirmaron que la proteína estimula la producción de insulina y que la conversión de proteína a glucosa es un proceso lento.
Problema: Los alimentos ricos en proteínas aumentan la secreción (producción) de insulina, incluso si los niveles de glucosa en sangre se mantienen relativamente constantes. Esto se debe a que ciertos aminoácidos estimulan directamente la secreción de insulina, sin requerir un aumento de glucosa. Esto significa que los alimentos ricos en proteínas desencadenan una respuesta insulínica tan fuerte como la de los alimentos ricos en carbohidratos.42,43,44,85 El aumento de la producción de insulina durante un período prolongado conduce a un agotamiento pancreático más rápido (disfunción de las células beta, estrés de las células beta).87
Varias revisiones sistemáticas sobre este tema concluyen que una dieta alta en proteínas no ofrece ninguna ventaja sobre el consumo moderado de proteínas.85,86
Además, una dieta rica en proteínas aumenta los niveles de IGF-1 en sangre. El factor de crecimiento similar a la insulina 1 es un factor de crecimiento similar a una hormona, estructuralmente similar a la insulina. Desempeña un papel importante en el crecimiento celular, el desarrollo tisular y la regeneración, e influye en el metabolismo de la glucosa en sangre. Favorece la acción de la insulina y ayuda a transportar la glucosa de la sangre a las células. El IGF-1 también activa la vía de señalización mTOR. Esta vía detecta la cantidad de aminoácidos, energía o estímulos de crecimiento disponibles y, posteriormente, decide si una célula debe crecer, dividirse o sintetizar proteínas. La sobreactivación sostenida se asocia con un crecimiento celular acelerado (p. ej., en el cáncer), procesos inflamatorios crónicos y una reducción de la autofagia (limpieza celular). La actividad reducida de mTOR (p. ej., mediante el ayuno, la restricción calórica y una menor ingesta de proteínas) se asocia claramente con un envejecimiento más saludable y una menor susceptibilidad a la inflamación.47
Un exceso de aminoácidos de cadena ramificada (BCAA como leucina, isoleucina y valina) también desestabiliza los receptores de insulina en las células musculares y adiposas. La captación de glucosa se reduce, lo que promueve la resistencia a la insulina.45 La combinación de aminoácidos (BCAA) y una dieta rica en grasas tiene un efecto similar. Además, provoca una acumulación de acilcarnitinas, que pueden ser tóxicas para los músculos y el hígado e inhibir la acción de la insulina.46
¿Consumo de alimentos “que reducen el azúcar en la sangre”?
Se conocen numerosos remedios caseros para la diabetes o para controlar los niveles de azúcar en sangre. Sin embargo, estas recomendaciones suelen basarse en resultados in vitro . o experimentos con animales. Cuando existen estudios en humanos, suelen ser breves, metodológicamente limitados o usar dosis excesivamente altas. Esto significa que apenas hay evidencia clínica sólida.
Estas sustancias se vuelven problemáticas cuando se utilizan como sustituto de cambios necesarios en la dieta y el estilo de vida. Sin duda, pueden ser un complemento, pero solo en el contexto de una dieta equilibrada y predominantemente vegetal .
El rábano picante (moringa) se considera una planta milagrosa para reducir los niveles de azúcar en sangre. Dos estudios en animales y tres en humanos han demostrado los efectos beneficiosos de las hojas de rábano picante en la diabetes tipo 2: reducen el colesterol, inhiben la inflamación y protegen las células pancreáticas. Además, el rábano picante contiene cuatro de los compuestos vegetales (fitoquímicos) más eficaces contra la hiperglucemia y la dislipidemia. Los grupos de estudio que consumieron una dosis diaria de polvo de hojas de rábano picante mostraron una reducción significativa de los marcadores de diabetes en comparación con los grupos de control que no tomaron suplementos de rábano picante.74
Se ha demostrado que una combinación de compuestos vegetales de arándanos, orégano, romero y Rhodiola rosea es eficaz en el tratamiento de la diabetes y mejora la función pancreática.16
Estudios aleatorizados, controlados con placebo y doble ciego en humanos han demostrado que el consumo de canela es otra forma útil de regular la glucemia y la presión arterial, ya que tomar al menos 2 g de canela durante 12 semanas reduce significativamente los principales marcadores de diabetes.75 Cabe destacar que la canela contiene cumarina, que es perjudicial para el hígado. Según el Instituto Federal Alemán para la Evaluación de Riesgos ( BfR ), la ingesta diaria tolerable (IDT) de cumarina es de 0,1 mg/kg de peso corporal.78 Puede encontrar más información en el apartado sobre el ingrediente canela .
Un estudio de cohorte realizado en Corea reveló que el consumo de algas se correlacionaba con un menor riesgo de diabetes.76 estudios en animales confirman el efecto de las algas. La Chlorella vulgaris previno el desarrollo de resistencia a la insulina en ratas.77
Frecuencia de las comidas
Numerosos estudios han demostrado el potencial del ayuno intermitente para combatir la diabetes. Las diversas formas de ayuno intermitente, como el 16:8 y el 5:2, conducen sistemáticamente a una reducción de la glucemia en ayunas, la HbA1c, el peso corporal y la resistencia a la insulina. Con el método 16:8, se come durante 8 horas y se ayuna durante las 16 horas restantes. Con el método 5:2, se ayuna durante 2 días y se come con normalidad durante 5 días.
El ayuno intermitente funciona mediante procesos como la autofagia, la cetogénesis, la reducción del estrés oxidativo y una mejora en la función de las células beta. Particularmente en la prediabetes, el ayuno intermitente puede estabilizar los procesos metabólicos y, por lo tanto, prevenir o retrasar la progresión a una enfermedad manifiesta.62,63,64 También es eficaz y seguro para las personas con diabetes tipo 2 tratadas con insulina.65
Una revisión sistemática de 2024 confirma que una dieta con solo 2 o 3 comidas al día y una ventana de alimentación diaria de menos de 10 horas puede mejorar tanto el peso corporal como el control de la glucemia en la diabetes tipo 2. Es beneficioso alinear la ingesta de alimentos con el ritmo natural del cuerpo. Saltarse el desayuno altera este ritmo. Un descanso de 3 a 4 horas después de una comida favorece la regulación de la glucemia.88
El ayuno intermitente no se recomienda para personas con diabetes tipo 1 porque aumenta el riesgo de hipoglucemia.
Sobrepeso y obesidad
El sobrepeso y la obesidad se consideran factores de riesgo clave para la diabetes. Si bien la diabetes tipo 2 se considera "diabetes del adulto", su prevalencia en niños ha aumentado desde 1990. Este fenómeno está directamente relacionado con el aumento de la obesidad infantil.48
Cuando aumenta el peso corporal, no crece la cantidad de células grasas, sino el tamaño de las existentes. La grasa se acumula dentro de estas células, provocando su agrandamiento. En cierto punto, la grasa se libera de las células y regresa al torrente sanguíneo, donde causa el mismo deterioro de la señalización de la insulina que una comida rica en grasas.
Incluso si una persona con sobrepeso lleva una dieta saludable, las células liberan grasa constantemente al torrente sanguíneo debido al efecto de derrame. Sin embargo, incluso en este caso, una persona que sigue una dieta a base de plantas, incluso con el mismo peso que un omnívoro, presenta una mejor sensibilidad a la insulina, mejores niveles de azúcar e insulina en sangre y una mejor función de las células pancreáticas.49
Utilice los siguientes valores para comprobar si tiene un mayor riesgo de desarrollar diabetes. Para mayor precisión, conviene combinar varios métodos.
Verifique su IMC y la relación cintura-cadera y cintura-altura.
El IMC (índice de masa corporal) es una fórmula desarrollada por Adolphe Quetelet en la década de 1850 para calcular la masa corporal.
Calcula tu IMC con esta fórmula: IMC = peso en kg / (altura en m x altura en m). Ejemplo: Altura 176 cm, peso 68 kg. 1,76 m x 1,76 m = 3,0976. 68 / 3,0976 = 21,952 = IMC 22.
Según la Organización Mundial de la Salud (OMS), un IMC de 18,5 a 24,9 kg/m2 se considera peso normal. Un IMC de 25 kg/m2 o superior se considera sobrepeso, y un IMC de 30 kg/m2 o superior se considera obesidad. Sin embargo, el IMC por sí solo es un indicador limitado de salud, ya que no tiene en cuenta la constitución corporal individual ni, en particular , la distribución de la masa corporal (grasa y tejido muscular).
Aunque este método es ampliamente utilizado y permite comparaciones precisas entre diferentes grupos, tiene varias desventajas:
- No tiene en cuenta si el peso proviene de masa muscular magra o grasa. Por lo tanto, sobreestima el riesgo para la salud en personas musculosas pero sanas, mientras que subestima el riesgo en personas de "peso normal" con un alto porcentaje de grasa corporal.
- No indica en qué parte del cuerpo se encuentra la grasa (la grasa visceral, que rodea los órganos, es más peligrosa que la grasa que se almacena debajo de la piel).
- No tiene en cuenta ni la edad ni el género (las mujeres tienen más depósitos de grasa que los hombres y las personas mayores más que las personas jóvenes).
El índice cintura-cadera proporciona información sobre la grasa visceral, especialmente peligrosa. Según la OMS, un índice cintura-cadera < 0,85 se considera óptimo para las mujeres y < 0,90 para los hombres. Por ejemplo, una persona con una circunferencia de cintura de 71 cm y una circunferencia de cadera de 84 cm tiene un índice cintura-cadera de 0,85 . Valores superiores a este valor se consideran obesidad abdominal.
Actualmente, el índice cintura-estatura se considera uno de los mejores indicadores de riesgos para la salud. Se calcula dividiendo la circunferencia de la cintura entre la estatura. Por ejemplo: 80 cm (circunferencia de la cintura) dividido entre 170 cm (estatura) = 0,47. Un valor < 0,5 se considera saludable, ≥ 0,5 un mayor riesgo y ≥ 0,6 un riesgo significativamente mayor.52
La pérdida de peso conduce a una mejor sensibilidad a la insulina.
Menos grasa corporal, especialmente en la zona abdominal, hace que las células del cuerpo sean más sensibles a la insulina. Esto reduce los niveles de azúcar en sangre, ya que la insulina existente puede actuar con mayor eficacia. Al mismo tiempo, un peso más bajo alivia la carga de las células beta del páncreas, que suelen estar sobrecargadas en la diabetes tipo 2. Estas tienen que trabajar menos horas extra y pueden recuperarse parcialmente, lo que estabiliza la producción de insulina. En general, la pérdida de peso se traduce en mejores niveles de azúcar en sangre, menor necesidad de medicación y menor riesgo de enfermedades secundarias. También reduce el efecto de derrame descrito anteriormente: el reflujo de grasa de las células al torrente sanguíneo en casos de sobrepeso.
Sin embargo, no deberías hacer una dieta drástica, sino un cambio a largo plazo en tus hábitos alimenticios. Puedes encontrar más información en nuestro artículo: Pérdida de peso saludable y sostenible.
¿Diabetes tipo 2 en personas delgadas?
La obesidad es ampliamente conocida como un factor de riesgo para la diabetes. Sin embargo, incluso las personas delgadas pueden desarrollarla. El problema es que esta concienciación está ampliamente ausente en la población general. Muchas personas delgadas se sienten "automáticamente sanas" y, por lo tanto, no se realizan pruebas, ignorando las señales de alerta tempranas. Como resultado, la diabetes a menudo pasa desapercibida en este grupo durante mucho tiempo, a menudo hasta que ya se han desarrollado trastornos metabólicos significativos o enfermedades secundarias. Entre los afectados se incluyen personas con baja masa muscular, poco ejercicio, distribución desfavorable de la grasa (mucha grasa visceral) y una dieta poco saludable. Estas personas también tienen un mayor riesgo de desarrollar diabetes.53,54,55,56
A estas personas de peso normal se les denomina "flacos gordos" o "TOFI", que se puede traducir como "delgado por fuera, gordo por dentro".
Taylor et al. (2015) plantearon la hipótesis de que cada persona tiene un límite individual de grasa que puede almacenar de forma segura. Superar este límite provoca depósitos de grasa en el hígado y el páncreas, lo que favorece la diabetes. Debido a este límite individual de grasa, incluso las personas con un peso normal pueden desarrollar diabetes. Su tesis: Estas personas también se benefician de la pérdida de peso.57
Una predisposición genética a una baja reserva de células beta también puede ser una causa. El páncreas se agota más rápidamente y produce poca o ninguna insulina, lo que provoca diabetes.58,59 Véase también MODY (Diabetes de inicio en la madurez en jóvenes).
También es importante descartar la diabetes tipo 1 de aparición tardía relacionada con el sistema inmunitario . Las pruebas de anticuerpos confirman si hay o no LADA (diabetes autoinmune latente en adultos).
Falta de ejercicio
Un estilo de vida sedentario con falta de ejercicio es uno de los principales factores de riesgo para la diabetes tipo 2. Según estudios de investigación, seguir un programa de ejercicio moderado y estructurado reduce los marcadores de diabetes (HA1c) en ocho semanas. Según el Instituto de Ciencias del Ejercicio Humano de la Universidad Old Dominion en Virginia, la combinación de entrenamiento de resistencia y fuerza es la más eficaz para regular los niveles de azúcar en sangre. Aumentar la masa muscular mejora la absorción de glucosa en la sangre y su uso como combustible, mientras que el ejercicio de resistencia mejora la función de la insulina.66
| Tipo de ejercicio | ¿Qué sucede en el cuerpo? |
| Entrenamiento de resistencia | Los músculos necesitan glucosa para funcionar, por lo que los niveles de glucosa en sangre disminuyen. Un solo entrenamiento aumenta la actividad de la insulina y la tolerancia a la glucosa durante más de 24 horas (hasta 72 horas). |
| Entrenamiento de fuerza | El resultado es un nivel de azúcar en sangre en ayunas más bajo 24 horas después del entrenamiento; el grado de reducción depende del alcance y la intensidad del entrenamiento. |
Se debe prestar especial atención a los pacientes con otras complicaciones de la diabetes (como trastornos circulatorios, neuropatía, retinopatía, etc.). Además, puede presentarse hiperglucemia o hipoglucemia durante el ejercicio si no se controlan los niveles de glucosa en sangre. En estos casos, se recomienda ajustar la medicación y realizar una monitorización estrecha.
Contaminantes orgánicos persistentes (COP)
Los COP son toxinas ambientales persistentes, como los insecticidas (DDT), los productos químicos industriales (bifenilos policlorados, PCB) o ciertos retardantes de llama (PBDE). Las dioxinas de los procesos de combustión también promueven la inflamación y tienen efectos similares a los de las hormonas.
Los estudios de cohorte de Zong et al. (2018) y Magliano et al. (2021) demuestran que los contaminantes orgánicos persistentes (COP) Se han identificado factores de riesgo claros e independientes para la diabetes tipo 2.69,70 Los COP no actúan como sustancias individuales, sino como mezclas químicas que se acumulan en el tejido adiposo. Alteran la secreción de insulina por las células beta y promueven la inflamación y la disfunción mitocondrial, mecanismos fundamentales para el desarrollo de la diabetes tipo 2. Incluso una baja exposición ambiental diaria a los COP es metabólicamente relevante y aumenta de forma sostenida el riesgo de diabetes tipo 2.71
Es importante evitar estas sustancias porque sus efectos son independientes del peso, el IMC, la circunferencia de la cintura o el estilo de vida. Incluso las personas con un peso y un estilo de vida saludables mostraron un riesgo significativamente mayor de diabetes cuando sus niveles de POP eran más altos.69,70
Los contaminantes químicos liberados al medio ambiente penetran en el organismo de los animales. Los humanos los ingieren a través de alimentos de origen animal. Estas toxinas, que los humanos almacenan en sus propias reservas de grasa, son responsables de desequilibrios hormonales, obesidad, resistencia a la insulina, enfermedad del hígado graso no alcohólico y, en consecuencia, diabetes. Una dieta vegana ayuda a evitar muchas fuentes de COP.
Conclusión
La diabetes tipo 1 es incurable porque el cuerpo ya no produce insulina (o produce muy poca). En la diabetes tipo 2, es posible normalizar los niveles de azúcar en sangre (remisión) en ciertas circunstancias. Especialmente en las primeras etapas de la enfermedad y con suficiente función pancreática residual, los cambios en la dieta y el estilo de vida suelen ser suficientes sin medicación. Otras personas inicialmente requieren medicación de apoyo. Sin embargo, la medicación por sí sola no es eficaz a largo plazo. Si bien alivia los síntomas, no trata la causa subyacente de la diabetes. Además, todos los medicamentos eficaces tienen efectos secundarios de diversa gravedad.
Los pacientes con diabetes tipo 2 deben tener cuidado de no afectar la función de la hormona insulina. Esta hormona regula la absorción de glucosa del torrente sanguíneo a las células. El exceso de grasa almacenada en las células musculares, el consumo de carbohidratos refinados y ácidos grasos saturados, la falta de actividad física, los contaminantes orgánicos y la inflamación en el cuerpo afectan el correcto funcionamiento de la insulina.
La Organización Mundial de la Salud (OMS) destaca que la diabetes se puede controlar mediante dieta, actividad física, medicación, exámenes regulares y tratamiento de las complicaciones, y que las consecuencias de la enfermedad se pueden evitar o retrasar.
Muchos estudios confirman la influencia de la dieta en la diabetes tipo 2. Sin embargo, según una encuesta, los profesionales médicos aconsejan solo a una de cada tres personas con prediabetes que haga más ejercicio y lleve una dieta más saludable.79
Los medicamentos pueden contribuir a la pérdida de peso, el control de la glucemia o el sistema cardiovascular. Sin embargo, según el estudio ACCORD, la reducción intensiva de la glucemia con medicamentos tiene el efecto contrario: la reducción agresiva de la HbA1c a niveles casi normales durante 3,5 años aumentó la mortalidad y no resultó en una reducción significativa de los eventos cardiovasculares mayores.80 Estos hallazgos resaltan que la reducción excesiva y rápida de la glucosa en pacientes de alto riesgo con diabetes tipo 2 plantea riesgos inesperados y previamente subestimados.
Los medicamentos suelen tener efectos secundarios. Por lo tanto, un cambio constante en la dieta y el estilo de vida, especialmente con un diagnóstico temprano y una buena función residual de las células beta, es una estrategia sensata para mantener estable la glucemia incluso sin medicación.
Una dieta saludable basada en plantas, como la descrita anteriormente, en combinación con entrenamiento de resistencia y fuerza, ayuno intermitente y pérdida de peso sostenible no solo es útil para prevenir la diabetes tipo 2, sino que en muchos casos también permite una mejora significativa en la salud metabólica, que incluso conduce a la remisión.
La terapia específica más adecuada depende de la situación individual.
Bibliografía - 96 Fuentes (Enlace a la evidencia)
| 1. | * Editorial / Expertinnenmeinung DOI: 10.1093/ndt/gfaf177 Study: weak evidence | Duncan BB, Magliano DJ, Boyko EJ. IDF Diabetes Atlas 11th edition 2025: global prevalence and projections for 2050. Nephrology Dialysis Transplantation. 2026;41(1):7-9. |
| 2. | * Narratives Review DOI: 10.1016/j.amjmed.2013.06.007 Study: weak evidence | Pratley RE. The early treatment of type 2 diabetes. Am J Med. 2013;126(9 Suppl 1):S2–S9. |
| 3. | ● Website | Diabetesschweiz ch: Diabetes Typ 2, Blutzucker-Grenzwerte Typ-2-Diabetes. |
| 4. | * Narratives Review DOI: 10.3390/biology14080981 Study: weak evidence | Kotsiri I, Xanthi M, Domazinaki CM, Magiorkinis E. The Role of Viral Infections in the Immunopathogenesis of Type 1 Diabetes Mellitus: A Narrative Review. Biology (Basel). 2025;14(8):981. |
| 5. | * Narratives Review DOI: 10.1038/s41574-020-00443-4 Study: weak evidence | Roep BO, Thomaidou S, et al. Type 1 diabetes mellitus as a disease of the β-cell (do not blame the immune system?). Nat Rev Endocrinol. 2021;17(3):150-161. |
| 6. | * Systematisches Review mit Meta-Analyse DOI: 10.2337/diacare.17.1.13 Study: strong evidence | Gerstein HC. Cow's milk exposure and type I diabetes mellitus: a critical overview of the clinical literature. Diabetes Care. 1994;17(1):13‑19. |
| 7. | * Prospektive Fall-Kontroll-Studie innerhalb einer Geburtskohorte DOI: 10.1002/dmrr.1294 Study: moderate evidence | Lempainen J, Tauriainen S, et al. Interaction of enterovirus infection and cow's milk-based formula nutrition in type 1 diabetes-associated autoimmunity. Diabetes Metab Res Rev. 2012 Feb;28(2):177-185. |
| 8. | * Narratives Review DOI: 10.2337/diabetes.48.8.1501 Study: weak evidence | Harrison LC, Honeyman MC. Cow's milk and type 1 diabetes: the real debate is about mucosal immune function. Diabetes. 1999 Aug;48(8):1501-1507. |
| 9. | * Fall‑Kontroll‑Studie + In‑silico‑Analyse DOI: 10.1080/07391102.2021.1953599 Study: moderate evidence | Benslama Y, Dennouni-Medjati N, et al. Childhood type 1 diabetes mellitus and risk factor of interactions between dietary cow's milk intake and HLA-DR3/DR4 genotype. J Biomol Struct Dyn. 2022;40(21):10931-10939. |
| 10. | * Querschnittsstudie (Cross‑sectional Study) DOI: 10.1016/j.nutres.2014.02.001 Study: moderate evidence | Hofe CR, Feng L, et al. Fruit and vegetable intake, as reflected by serum carotenoid concentrations, predicts reduced probability of PCB-associated risk for type 2 diabetes: NHANES 2003–2004. Nutr Res. 2014;34(4):285–293. |
| 11. | * Randomisierte kontrollierte Interventionsstudie (RCT) Results Forty-three per cent of participants in the experimental group and 5% of participants in the control group reduced diabetes medication (P < 0.001). Body weight decreased more in the experimental group than in the control group [–6.2 kg (95% CI –6.6 to –5.3) vs. –3.2 kg (95% CI –3.7 to –2.5); interaction group × time P = 0.001]. An increase in insulin sensitivity was significantly greater in the experimental group than in the control group [30% (95% CI 24.5–39) vs. 20% (95% CI 14–25), P = 0.04]. A reduction in both visceral and subcutaneous fat was greater in the experimental group than in the control group (P = 0.007 and P = 0.02, respectively). Plasma adiponectin increased (P = 0.02) and leptin decreased (P = 0.02) in the experimental group, with no change in the control group. Vitamin C, superoxide dismutase and reduced glutathione increased in the experimental group (P = 0.002, P < 0.001 and P = 0.02, respectively). Differences between groups were greater after the addition of exercise training. Changes in insulin sensitivity and enzymatic oxidative stress markers correlated with changes in visceral fat. DOI: 10.1111/j.1464-5491.2010.03209.x Study: strong evidence | Kahleova H, Matoulek M, et al. Vegetarian diet improves insulin resistance and oxidative stress markers more than conventional diet in subjects with Type 2 diabetes. Diabet Med. 2011 May;28(5):549-559. |
| 12. | * DOI: 10.1111/dme.12032 Study: strong evidence | Kahleova H, Hrachovinova T, Hill M, Pelikanova T. Vegetarian diet in type 2 diabetes--improvement in quality of life, mood and eating behaviour. Diabet Med. 2013;30(1):127-129. |
| 13. | * Prospektive Kohortenstudie DOI: 10.2337/dc08-1325 Study: moderate evidence | Liese AD, Weis KE, et al. Food Intake Patterns Associated With Incident Type 2 Diabetes: The Insulin Resistance Atherosclerosis Study. Diabetes Care. 2009;32(2):263-268. |
| 14. | * Narratives Review DOI: 10.2147/DMSO.S9089 Study: weak evidence | Badawi A, Klip A, et al. Type 2 diabetes mellitus and inflammation: Prospects for biomarkers of risk and nutritional intervention. Diabetes Metab Syndr Obes. 2010;3:173–186. |
| 15. | * Systematisches Review und Meta-Analyse von RCT DOI: 10.1007/s00125-009-1395-7 Study: strong evidence | Sievenpiper JL, Kendall CW, et al. Effect of non-oil-seed pulses on glycaemic control: a systematic review and meta-analysis of randomised controlled experimental trials in people with and without diabetes. Diabetologia. 2009;52(8):1479-1495. |
| 16. | ● Book | Clement, B. Food Is Medicine. The Scientific Evidence. Summertown, Hippocrates Publications; 2012. |
| 17. | * Prospektive Kohortenstudie (Analyse von drei grossen US‑Kohorten: NHS, NHS II, HPFS) DOI: 10.1371/journal.pmed.1002039 Study: moderate evidence | Satija A, Bhupathiraju SN, et al. Plant-Based Dietary Patterns and Incidence of Type 2 Diabetes in US Men and Women: Results from Three Prospective Cohort Studies. PLoS Medicine. 2016;13(6):e1002039. |
| 18. | * Experimentelle Interventionsstudie am Menschen DOI: 10.1172/JCI118742 Study: moderate evidence | Roden M, Price TB, et al. Mechanism of free fatty acid-induced insulin resistance in humans. J Clin Invest. 1996;97(12):2859–2865. |
| 19. | * Experimentelle Human‑Interventionsstudie DOI: 10.2337/diabetes.48.2.358 Study: moderate evidence | Roden M, Krssak M, et al. Rapid impairment of skeletal muscle glucose transport/phosphorylation by free fatty acids in humans. Diabetes. 1999;48(2):358–364. |
| 20. | * Experimentelle Human‑Interventionsstudie DOI: 10.2337/diabetes.48.9.1836 Study: moderate evidence | Santomauro AT, Boden G, et al. Overnight lowering of free fatty acids with Acipimox improves insulin resistance and glucose tolerance in obese diabetic and nondiabetic subjects. Diabetes. 1999;48(9):1836–1841. |
| 21. | * Querschnittsstudie DOI: 10.1007/s001250051123 Study: moderate evidence | Krssak M, Falk Petersen K, et al. Intramyocellular lipid concentrations are correlated with insulin sensitivity in humans: a 1H NMR spectroscopy study. Diabetologia. 1999;42(1):113–116. |
| 22. | * Querschnittstudie DOI: 10.2337/dc08-1886 Study: moderate evidence | Tonstad S, Butler T, Yan R, Fraser GE. Type of vegetarian diet, body weight, and prevalence of type 2 diabetes. Diabetes Care. 2009;32(5):791–796. |
| 23. | * Prospektive Kohortenstudie DOI: 10.3945/ajcn.2009.28713 Study: moderate evidence | Vergnaud AC, Norat T, et al. Meat consumption and prospective weight change in participants of the EPIC-PANACEA study. Am J Clin Nutr. 2010;92(2):398–407. |
| 24. | * Narrative Review DOI: 10.3945/ajcn.2010.28701F Study: moderate evidence | Sabaté J, Wien M. Vegetarian diets and childhood obesity prevention. Am J Clin Nutr. 2010;91(5):1525S–1529S. |
| 25. | * Narrative Review DOI: 10.1111/joim.13728 Study: moderate evidence | Hu FB. Diet strategies for promoting healthy aging and longevity: An epidemiological perspective. J Intern Med. 2024;295(4):508-531. |
| 26. | * Prospektive Kohortenstudie DOI: 10.2337/dc09-1321 Study: moderate evidence | Sluijs I, Beulens JW, et al. Dietary intake of total, animal, and vegetable protein and risk of type 2 diabetes in the European Prospective Investigation into Cancer and Nutrition (EPIC)-NL study. Diabetes Care. 2010;33(1):43-48. |
| 27. | * Systematisches Review und Meta-Analyse DOI: 10.1016/j.clnu.2024.07.001 Study: strong evidence | Fotouhi Ardakani A, Anjom-Shoae J, et al. Association between total, animal, and plant protein intake and type 2 diabetes risk in adults: A systematic review and dose-response meta-analysis of prospective cohort studies. Clin Nutr. 2024;43(8):1941-1955. |
| 28. | * Kohortenstudie (Rotterdam Study) und Systematisches Review + Meta-Analyse DOI: 10.1007/s10654-020-00607-6 Study: strong evidence | Chen Z, Glisic M, et al. Dietary protein intake and all-cause and cause-specific mortality: results from the Rotterdam Study and a meta-analysis of prospective cohort studies. Eur J Epidemiol. 2020;35(5):411-429. |
| 29. | * Systematisches Review und Meta-Analyse DOI: 10.1161/CIRCULATIONAHA.109.924977 Study: strong evidence | Micha R, Wallace SK, et al. Red and processed meat consumption and risk of incident coronary heart disease, stroke, and diabetes mellitus. Circulation. 2010;121(21):2271-2283. |
| 30. | * Eine experimentelle Labor- und Methodenstudie DOI: 10.1016/j.jada.2010.03.018 Study: weak evidence | Uribarri J, Woodruff S, et al. Advanced glycation end products in foods and a practical guide to their reduction in the diet. J Am Diet Assoc. 2010;110(6):911-916.e12. |
| 31. | * Prospektive Kohortenstudie DOI: 10.1038/s42255-024-01109-5 Study: moderate evidence | Wang F, Glenn AJ et al. Integration of epidemiological and blood biomarker analysis links haem iron intake to increased type 2 diabetes risk. Nat Metab. 2024;6(9):1807–1818. |
| 32. | * prospektive Kohortenstudie DOI: 10.3945/ajcn.115.108712 Study: moderate evidence | Bao W, Chavarro JE, et al. Long-term risk of type 2 diabetes in relation to habitual iron intake in women with a history of gestational diabetes: a prospective cohort study. Am J Clin Nutr. 2016;103(2):375-381. |
| 33. | * Prospektive Kohortenstudie DOI: 10.2337/dc06-0119 Study: moderate evidence | Rajpathak S, Ma J, et al. Iron intake and the risk of type 2 diabetes in women: a prospective cohort study. Diabetes Care. 2006;29(6):1370-1376. |
| 34. | * Multimodale experimentelle Studie DOI: 10.1038/nm.3145 Study: weak evidence | Koeth RA, Wang Z, et al. Intestinal microbiota metabolism of l-carnitine, a nutrient in red meat, promotes atherosclerosis. Nat Med. 2013;19(5):576-585. |
| 35. | ● Book | Hyman M. The Blood Sugar Solution. New York, Hyman Enterprises, 2012 |
| 36. | * Systematisches Review DOI: 10.3945/an.114.007690 Study: strong evidence | Pasin G, Comerford KB. Dairy Foods and Dairy Proteins in the Management of Type 2 Diabetes: A Systematic Review of the Clinical Evidence. Advances in Nutrition. 2015;6(3):245-259. |
| 37. | * Narratives Review DOI: 10.1186/1743-7075-10-46 Study: weak evidence | McGregor RA, Poppitt SD. Milk protein for improved metabolic health: a review of the evidence. Nutr Metab. 2013;10:46 |
| 38. | * prospektive Kohortenstudie DOI: 10.2337/dc06-0256 Study: moderate evidence | Liu S, Choi HK, et al. A Prospective Study of Dairy Intake and the Risk of Type 2 Diabetes in Women. Diabetes Care 2006;29(7):1579-1584. |
| 39. | * Systematisches Review + Meta-Analyse von Kohortenstudien DOI: 10.1038/ejcn.2011.62 Study: strong evidence | Tong X, Dong JY, et al. Dairy consumption and risk of type 2 diabetes mellitus: a meta-analysis of cohort studies. Eur J Clin Nutr 2011;65:1027–1031. |
| 40. | * Systematisches Review und Meta-Analyse DOI: 10.1371/journal.pone.0073965 Study: strong evidence | Gao D, Ning N, et al. Dairy Products Consumption and Risk of Type 2 Diabetes: Systematic Review and Dose-Response Meta-Analysis. PLoS ONE. 2013;8(9):e73965. |
| 41. | * Systematisches Review und Meta-Analyse von Kohortenstudien DOI: 10.3945/ajcn.113.059030 Study: strong evidence | Aune D, Norat T, et al. Dairy products and the risk of type 2 diabetes: a systematic review and dose-response meta-analysis of cohort studies. Am J Clin Nutr. 2013;98:1066–1083. |
| 42. | * Narratives Review DOI: 10.2337/dci24-0096 Study: weak evidence | Dao GM, Kowalski GM, et al. The Glycemic Impact of Protein Ingestion in People With Type 1 Diabetes. Diabetes Care. 2025;48(4):509-518. |
| 43. | * Experimentelle Humanstudie (akute Stoffwechselstudie) DOI: 10.1093/ajcn/66.5.1264 Study: weak evidence | Holt SH, Miller JC, Petocz P. An insulin index of foods: the insulin demand generated by 1000-kJ portions of common foods. Am J Clin Nutr. 1997;66(5):1264-1276. |
| 44. | * Narrative Review DOI: 10.1042/CS20040290 Study: weak evidence | Newsholme P, Brennan L, et al. New insights into amino acid metabolism, beta-cell function and diabetes. Clin Sci. 2005;108(3):185-194. |
| 45. | * Narratives Review DOI: 10.1038/nrendo.2014.171 Study: weak evidence | Lynch CJ, Adams SH. Branched-chain amino acids in metabolic signalling and insulin resistance. Nat Rev Endocrinol. 2014;10(12):723-736. |
| 46. | * Tier‑Interventionsstudien DOI: 10.1016/j.cmet.2009.02.002 Study: weak evidence | Newgard CB, An J, et al. A branched-chain amino acid-related metabolic signature that differentiates obese and lean humans and contributes to insulin resistance. Cell Metab. 2009;9(4):311-326. |
| 47. | * Narratives Review DOI: 10.1038/nature11861 Study: weak evidence | Johnson SC, Rabinovitch PS, et al. mTOR is a key modulator of ageing and age-related disease. Nature. 2013 Jan 17;493(7432):338-345. |
| 48. | * Narratives Review DOI: 10.1542/peds.2004-2536 Study: weak evidence | Hannon TS, Rao G, Arslanian SA. Childhood obesity and type 2 diabetes mellitus. Pediatrics. 2005;116(2):473–480. |
| 49. | * Fall‑Kontroll‑Studie DOI: 10.1038/sj.ejcn.1602076 Study: moderate evidence | Goff LM, Bell JD, et al. Veganism and its relationship with insulin resistance and intramyocellular lipid. Eur J Clin Nutr. 2005;59(2):291–298. |
| 50. | ● Website | WHO. A healthy lifestyle - WHO recommendations. Mai 2010. |
| 51. | ● Website | Report of a WHO Expert Consultation. Waist Circumference and Waist-Hip Ratio. Geneva 2008. |
| 52. | * Querschnittsstudie DOI: 10.1136/bmjopen-2015-010159 Study: moderate evidence | Ashwell M, Gibson S. Waist‑to‑height ratio as an indicator of ‘early health risk’: simpler and more predictive than using a ‘matrix’ based on BMI and waist circumference. BMJ Open. 2016;6(3):e010159. |
| 53. | * Narratives Review mit Meta‑Analyse DOI: 10.1007/s11892-024-01559-x Study: weak evidence | Bai J, Zhang Y, et al. Normal Weight Central Obesity and its Impact on Type 2 Diabetes Mellitus. Curr Diab Rep. 2025;25:3. |
| 54. | * Querschnittsstudie DOI: 10.3389/fnut.2023.1239493 Study: moderate evidence | Jin X, Liu J, et al. Normal-weight central obesity: implications for diabetes mellitus. Front Nutr. 2023;10:1239493. |
| 55. | * Querschnittsstudie DOI: 10.1016/j.numecd.2018.06.015 Study: moderate evidence | Xu S, Ming J, et al. Normal weight obesity and the risk of diabetes in Chinese people: a 9-year population-based cohort study. Sci Rep. 2021;11(1):6090. |
| 56. | * Narratives Review DOI: 10.3390/ijerph19020624 Study: weak evidence | Pluta W, Dudzińska W, Lubkowska A. Metabolic Obesity in People with Normal Body Weight (MONW)-Review of Diagnostic Criteria. Int J Environ Res Public Health. 2022 Jan 6;19(2):624. |
| 57. | * Hypothesenpapier / Expertenmeinung DOI: 10.1042/CS20140553 Study: weak evidence | Taylor R, Holman RR. Normal weight individuals who develop type 2 diabetes: the personal fat threshold. Clin Sci (Lond). 2015;128(7):405-410. |
| 58. | * Prospektive Kohortenstudie DOI: 10.1016/j.diabres.2025.112049 Study: moderate evidence | Morita S, Shimajiri Y, Matsuoka Y, Kadoya Y, Yamada S, Matsuoka TA, Sanke T. Exploring genetic risk factors for β-cell deterioration in type 2 diabetes mellitus: Insights from longitudinal C-peptide analysis. Diabetes Res Clin Pract. 2025;222:112049. |
| 59. | * Narratives Review DOI: 10.1126/science.110434 Study: weak evidence | Rhodes CJ. Type 2 Diabetes—a Matter of β-Cell Life and Death? Science. 2005;307(5708):380‑384. |
| 60. | * Experimentelle physiologische Humanstudie mit intensiver metabolischer Charakterisierung DOI: 10.2337/dc21-1957 Study: weak evidence | Lontchi-Yimagou E, Dasgupta R, et al. An Atypical Form of Diabetes Among Individuals With Low BMI. Diabetes Care. 2022;45(6):1428-1437. |
| 61. | * Narratives Review DOI: 10.1152/physiol.00065.202 Study: weak evidence | Wadivkar P, Thomas N, Jebasingh F, Bacot-Davis VR, Maini R, Hawkins M. Undernutrition-Associated Diabetes Mellitus: Pathophysiology of a Global Problem. Physiology (Bethesda). 2025 Sep 1;40(5):0. |
| 62. | * Narratives Review DOI: 10.3389/fnut.2025.1629154 Study: weak evidence | Dyńka D, Rodzeń L, et al. Intermittent fasting in the treatment of type 2 diabetes. Front Nutr. 2025;12:1629154. |
| 63. | * Systematisches Review und Meta-Analyse DOI: 10.1210/clinem/dgaa926 Study: strong evidence | Borgundvaag E, Mak J, Kramer CK. Metabolic Impact of Intermittent Fasting in Patients With Type 2 Diabetes Mellitus: A Systematic Review and Meta-analysis. J Clin Endocrinol Metab. 2021;106(3):902–911. |
| 64. | * Narratives Review DOI: 10.3390/nu16162692 Study: weak evidence | Msane S, Khathi A, Sosibo A. Therapeutic Potential of Various Intermittent Fasting Regimens in Alleviating Type 2 Diabetes Mellitus and Prediabetes: A Narrative Review. Nutrients. 2024;16(16):2692. |
| 65. | * Randomisierte kontrollierte Studie (RCT) DOI: 10.2337/dc22-1622 Study: strong evidence | Obermayer A, Tripolt NJ, et al. Efficacy and Safety of Intermittent Fasting in People With Insulin‑Treated Type 2 Diabetes (INTERFAST‑2). Diabetes Care. 2022;46(2):463–472. |
| 66. | * Expertenmeinung / Positionspapier DOI: 10.2337/dc10-9990 Study: weak evidence | Colberg SR, Sigal RJ, et al. Exercise and Type 2 Diabetes: The American College of Sports Medicine and the American Diabetes Association: joint position statement. Diabetes Care. 2010;33(12):e147-e167. |
| 67. | * Systematisches Review DOI: 10.1016/j.diabet.2013.09.006 Study: strong evidence | Magliano DJ, Loh VHY, et al. Persistent organic pollutants and diabetes: a review of the epidemiological evidence. Diabetes Metab. 2014;40(1):1–14. |
| 68. | ● Website | ATSDR (Agency for Toxic Substances and Disease Registry): Toxicological Profile for Polychlorinated Biphenyls (PCBs. 2011. |
| 69. | * Prospektive, Fall-Kontroll‑Studie innerhalb einer Kohorte DOI: 10.1016/j.envint.2017.12.010 Study: moderate evidence | Zong G, Valvi D, et al. Persistent organic pollutants and risk of type 2 diabetes: A prospective investigation among middle-aged women in Nurses' Health Study II. Environ Int. 2018;114:334-342. |
| 70. | * Fall-Kontroll-Studie DOI: 10.1016/j.diabet.2021.101234 Study: moderate evidence | Magliano DJ, Rancière F, et al. Exposure to persistent organic pollutants and the risk of type 2 diabetes: a case-cohort study. Diabetes Metab. 2021;47(5):101234. |
| 71. | * Narratives Review DOI: 10.3389/fendo.2018.00712 Study: weak evidence | Lee YM, Jacobs DR Jr, Lee DH. Persistent Organic Pollutants and Type 2 Diabetes: A Critical Review of Review Articles. Front Endocrinol (Lausanne). 2018;9:712. |
| 72. | * Narrative Review DOI: 10.1038/nutd.2017.16 Study: weak evidence | Chia JSJ, McRae JL, Kukuljan S, Woodford K, Elliott RB, Swinburn B, Dwyer KM. A1 beta-casein milk protein and other environmental pre-disposing factors for type 1 diabetes. Nutr Diabetes. 2017;7(5):e274. |
| 73. | * Narratives Review DOI: 10.1007/s42399-021-00792-9 Study: weak evidence | Catanzaro R, Sciuto M, Marotta F. Lactose Intolerance—Old and New Knowledge on Pathophysiological Mechanisms, Diagnosis, and Treatment. SN Compr Clin Med. 2021;3:499‑509. |
| 74. | * Narratives Review DOI: 10.3389/fphar.2012.00024 Study: weak evidence | Mbikay M. Therapeutic Potential of Moringa oleifera Leaves in Chronic Hyperglycemia and Dyslipidemia: A Review. Front Pharmacol. 2012;3:24. |
| 75. | * Systematisches Review mit Meta-Analyse DOI: 10.1370/afm.1517 Study: strong evidence | Allen RW, Schwartzman E, et al. Cinnamon use in type 2 diabetes: an updated systematic review and meta-analysis. Ann Fam Med. 2013;11(5):452-459. |
| 76. | * Kohortenstudie DOI: 10.1017/S0007114523002751 Study: moderate evidence | Kim C, Park K. Association between seaweed intake and risk of type 2 diabetes mellitus: a prospective cohort study. Br J Nutr. 2024 Apr 14;131(7):1259-1267. |
| 77. | * Experimentelle Tierstudie (in‑vivo) mit Ratten DOI: 10.1002/ptr.3379 Study: weak evidence | Chiu YJ, Chung HH, et al. Improvement of insulin resistance by Chlorella in fructose-rich chow-fed rats. Phytother Res. 2011;25(9):1306-1312. |
| 78. | ● Website | Bundesinstitut für Risikobewertung (BfR): Neue Erkenntnisse zu Cumarin in Zimt - Stellungnahme Nr. 036/2012 des BfR vom 27. September 2012. |
| 79. | * Querschnittsstudie (cross‑sectional study) auf Basis von NHANES‑Daten DOI: 10.2337/dc09-1957 Study: moderate evidence | Karve A, Hayward RA. Prevalence, diagnosis, and treatment of impaired fasting glucose and impaired glucose tolerance in nondiabetic U.S. adults. Diabetes Care. 2010;33(11):2355-2359. |
| 80. | * Randomisierte kontrollierte Studie (RCT) DOI: 10.1056/NEJMoa0802743 Study: strong evidence | Action to Control Cardiovascular Risk in Diabetes Study Group, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med. 2008;358(24):2545-2559. |
| 81. | * Randomisierte kontrollierte Studie DOI: 10.1007/s00125-024-06272-8 Study: strong evidence | Hanick CJ, Peterson CM, et al. A whole-food, plant-based intensive lifestyle intervention improves glycaemic control and reduces medications in individuals with type 2 diabetes: a randomised controlled trial. Diabetologia. 2025;68(2):308-319. |
| 82. | * Systematisches Review mit Meta-Analyse This study demonstrated that vegetarian or vegan diets were associated with lowering HbA1c, BMI, and LDL-C in a population with T2DM. Compared with lacto- vegetarian diets, vegan diets demonstrated more signifi cant effects on improving metabolic health. In conclu sion, this study highlights the preventive effect of a vegetarian or vegan diet on CVDs in individuals with T2DM. In the future, the proportion of components that make up a plant-based diet should be explored. DOI: 10.1093/nutrit/nuaf011 Study: strong evidence | Lv M, Mao J, et al. Effects of Vegetarian or Vegan Diets on Glycemic and Cardiometabolic Health in Type 2 Diabetes: A Systematic Review and Meta-analysis. Nutr Rev. 2025;83(8):1438-1449. |
| 83. | * Cross-Over-Studie BACKGROUND. Dietary intake of saturated fat is a likely contributor to nonalcoholic fatty liver disease (NAFLD) and insulin resistance, but the mechanisms that initiate these abnormalities in humans remain unclear. We examined the effects of a single oral saturated fat load on insulin sensitivity, hepatic glucose metabolism, and lipid metabolism in humans. Similarly, initiating mechanisms were examined after an equivalent challenge in mice. METHODS. Fourteen lean, healthy individuals randomly received either palm oil (PO) or vehicle (VCL). Hepatic metabolism was analyzed using in vivo 13C/31P/1H and ex vivo 2H magnetic resonance spectroscopy before and during hyperinsulinemic-euglycemic clamps with isotope dilution. Mice underwent identical clamp procedures and hepatic transcriptome analyses. RESULTS. PO administration decreased whole-body, hepatic, and adipose tissue insulin sensitivity by 25%, 15%, and 34%, respectively. Hepatic triglyceride and ATP content rose by 35% and 16%, respectively. Hepatic gluconeogenesis increased by 70%, and net glycogenolysis declined by 20%. Mouse transcriptomics revealed that PO differentially regulates predicted upstream regulators and pathways, including LPS, members of the TLR and PPAR families, NF-κB, and TNF-related weak inducer of apoptosis (TWEAK). CONCLUSION. Saturated fat ingestion rapidly increases hepatic lipid storage, energy metabolism, and insulin resistance. This is accompanied by regulation of hepatic gene expression and signaling that may contribute to development of NAFLD. DOI: 10.1172/JCI89444 Study: moderate evidence | Hernández EÁ, Kahl S, et al. Acute dietary fat intake initiates alterations in energy metabolism and insulin resistance. J Clin Invest. 2017;127(2):695-708. |
| 84. | * Randomisierte, kontrollierte Interventionsstudie DOI: 10.1007/s001250051620 Study: strong evidence | Vessby B, Uusitupa M, et al. Substituting dietary saturated for monounsaturated fat impairs insulin sensitivity in healthy men and women: The KANWU Study. Diabetologia. 2001;44(3):312-319. |
| 85. | * Systematisches Review DOI: 10.1093/advances/nmz002 Study: strong evidence | Malaeb S, Bakker C, et al. High-Protein Diets for Treatment of Type 2 Diabetes Mellitus: A Systematic Review. Adv Nutr. 2019;10(4):621-633. |
| 86. | * Systematisches Review DOI: 10.2337/dc11-2216 Study: strong evidence | Wheeler ML, Dunbar SA, et al. Macronutrients, food groups, and eating patterns in the management of diabetes: a systematic review of the literature, 2010. Diabetes Care. 2012;35(2):434-445. |
| 87. | ●
However, when demand for insulin chronically increases, a steady stimulation of β-cells eventually may lead to death. In spite of the conducted efforts in order to elucidate the glucotoxicity mechanisms acting on β-cells, they remain largely unknown.
DOI: 10.1007/978-3-031-25519-9_13 Book | Camarillo CO. Dysfunction and Death of Pancreatic Beta-Cells in Type 2 Diabetes. In: Rodriguez-Saldana J (Ed.). The Diabetes Textbook. Cham: Springer;2023. |
| 88. | * DOI: 10.1371/journal.pone.0298531 Study: strong evidence | Gómez-Ruiz RP, Cabello-Hernández AI, et al. Meal frequency strategies for the management of type 2 diabetes subjects: A systematic review. PLoS One. 2024;19(2):e0298531. |
| 89. | * Umbrella-Review (Zusammenfassung mehrerer systematischer Reviews + Meta-Analysen) DOI: 10.1093/advances/nmy107 Study: strong evidence | Alvarez-Bueno C, Cavero-Redondo I, et al. Effects of Milk and Dairy Product Consumption on Type 2 Diabetes: Overview of Systematic Reviews and Meta-Analyses. Adv Nutr. 2019;10(suppl_2):S154-S163. |
| 90. | * Meta-Analyse DOI: 10.1093/jn/nxaa447 Study: strong evidence | Pearce M, Fanidi A, et al. Associations of Total Legume, Pulse, and Soy Consumption with Incident Type 2 Diabetes: Federated Meta-Analysis of 27 Studies from Diverse World Regions. J Nutr. 2021;151(5):1231-1240. |
| 91. | * prospektive Beobachtungsstudie Using ambulatory assessment in everyday life, we were able to show that stress had a significant effect on blood glucose levels in IR individuals. This finding emphasises the need for preventive measures targeting stress levels, especially in IR individuals, to counteract mechanisms that trigger the dysregulation of blood sugar levels and promote disease progression. By integrating stress assessment, CGM insights and stress mitigation techniques into routine care, providers can better guide individuals to avert or delay type 2 diabetes, ultimately improving long-term health outcomes. DOI: 10.1007/s00125-025-06552-x Study: moderate evidence | Schrems E, Gruber JR, Schiweck C, Ruf A, Reif A, Goldbach R et al. Daily life stress is linked to increased glucose levels in individuals with insulin resistance: a real-world assessment. Diabetologia. 2025;68(12):2709–2718. |
| 92. | * prospektive Kohortenstudie In conclusion, in a study involving 73,630 adults wearing wrist wearables and observed for an average of 7.7 years, both irregular and moderately irregular sleep patterns were associated with higher T2D incidence. Notably, adhering to sleep duration recommendations did not offset the adverse effects of irregular or moderately irregular sleep patterns on T2D incidence. Conversely, individuals who did not meet sleep duration recommendations but maintained regular sleep patterns did not show an elevated risk of T2D incidence. These findings support the importance of including or giving more prominence to sleep regularity in public health guidelines and clinical practices for T2D prevention and management. Future studies should investigate whether interventions targeting improved sleep regularity could yield better outcomes in relation to T2D. DOI: 10.2337/dc24-1208 Study: moderate evidence | Chaput JP, Biswas RK, Ahmadi M, Cistulli PA, Sabag A, St-Onge MP et al. Sleep irregularity and the incidence of type 2 diabetes: a device-based prospective study in adults. Diabetes Care. 2024;47(12):2139–2145. |
| 93. | * Narratives Review Epidemiological studies demonstrate a clear association between cigarette smoking and an increased risk of T2D, whereas clinical data suggest an effect of smoking and nicotine on body composition, insulin sensitivity, and pancreatic β cell function. Human, rodent, and in vitro studies have begun to yield insight into the molecular mechanisms through which nicotine and smoking exposure impact glucose homeostasis. However, a complete understanding of the underlying pathways impacted by tobacco abuse, especially mechanistic studies focused on the pancreatic β cell, are lacking. Not withstanding these unknowns, this comprehensive review of available literature suggests that smoking should be elevated to the category of a recognized and modifiable risk factor for the development of diabetes, uniformly across all diabetes organizations and that smoking status should be considered as an indication for diabetes screening. Moreover, smoking cessation along with weight control post cessation should be promoted as an essential public health practice for diabetes prevention. DOI: 10.1016/j.trsl.2017.02.004 Study: weak evidence | Maddatu J, Anderson-Baucum E, Evans-Molina C. Smoking and the risk of type 2 diabetes. Transl Res. 2017;184:101-107. |
| 94. | * Narratives Review DOI: 10.1007/s00508-023-02161-z Study: weak evidence | Brath H, Kaser S, Tatschl C, Fischer-See S, Fasching P. Rauchen, erhitzte Tabakprodukte, Alkohol und Diabetes mellitus (Update 2023) [Smoking, heated tobacco products, alcohol and diabetes mellitus (update 2023)]. Wien Klin Wochenschr. 2023;135(Suppl 1):84-90. |
| 95. | * Narratives Review DOI: 10.4093/dmj.2012.36.2.108 Study: weak evidence | Kim SJ, Kim DJ. Alcoholism and diabetes mellitus. Diabetes Metab J. 2012;36(2):108. |
| 96. | ● Website | WHO World Health Organization: No level of alcohol consumption is safe for our health. 2023. |
| Hemos categorizado estudios y libros sobre nutrición y salud de acuerdo con las siguientes 3 categorías de evidencia: verde = evidencia sólida, amarillo = evidencia media, morado = evidencia débil. El resto de las fuentes están marcadas en gris. Puede encontrar una explicación detallada en nuestro artículo: ¿Ciencia o creencia? Cómo evaluar publicaciones. | ||

Comentarios