Образ жизни родителей: эпигенетическое воздействие на детей
Как питание и образ жизни родителей эпигенетически влияют на их будущих детей. Мы недооцениваем эпигенетическое воздействие.
Оглавление
Вывод
Nutritional Programming, то есть "Программирование питанием", описывает предрасположенность людей, к различным заболеваниям во взрослой жизни. Основные причины этого - изменения в развитии во внутриутробной фазе и в раннем детстве.
Согласно парадигме Баркера "Эволюционные истоки здоровья и болезней" ("Developmental Origins of Health and Disease"), условия в период периконцепции (за 2-3 месяца до беременности), а также беременность и фаза лактации очень сильно влияют на рождённых в будущем людей. Неблагоприятная окружающая среда вызывает предрасположенность к определённым, особенно воспалительным, заболеваниям, которые проявляются позже во взрослой жизни.1
Переедание и недоедание являются важными факторами, которые создают вредную среду для будущего ребенка. Они напрямую связаны с метаболическими состояниями, такими как высокое кровяное давление, инсулинорезистентность, гиперлипемия и абдоминальное ожирение. 2
Если окружающая среда вредна, эмбрион, плод или новорожденный адаптируются, чтобы выжить в этих неблагоприятных условиях. Эти изменения влияют на функции организма, ремоделирование тканей, активацию или отключение определённых генов. Они могут сохраняться или оставаться активными, даже если вредные раздражители исчезают.
Недоедание во время беременности и в раннем детстве может увеличить риск ожирения, диабета, метаболического синдрома и сердечно-сосудистых заболеваний в более позднем возрасте. При условии нездорового питания и низкой физической активности.3
Краткий глоссарий
Эмбрион: после того, как яйцеклетка оплодотворена спермой (зигота), она начинает делиться, пока не становится похожей на клеточный шар (бластоцисту) и перемещается в матку. Здесь одни из этих клеток образуют плаценту, а другие развиваются в эмбрион. Именно на этом этапе формируется большая часть внутренних органов и строения тела. Развитие головного и спинного мозга происходит на протяжении всей беременности. Новые клетки мозга развиваются как во время беременности, так и в первый год после рождения.
Плод: с конца 8-й недели после оплодотворения (10-я неделя беременности) и до рождения эмбрион называется плодом.
Плацента: орган, который формируется в матке беременной женщины и соединяет плод с матерью. Так переносятся питательные вещества и кислород. Он помогает удалять продукты жизнедеятельности из крови ребенка и бороться с инфекциями.
Беременность/зачатие: период между зачатием и рождением, когда эмбрион/плод развивается в утробе матери.
1. Питание родителей влияет на здоровье и благополучие их детей
Многим обывателям и учёным хорошо известно и они признают, что диета и образ жизни имеют прямое влияние на здоровье.
Новые исследования3 показывают, что личные пищевые привычки и физическая активность также определяют фактическое состояние здоровья и благополучия человека через:
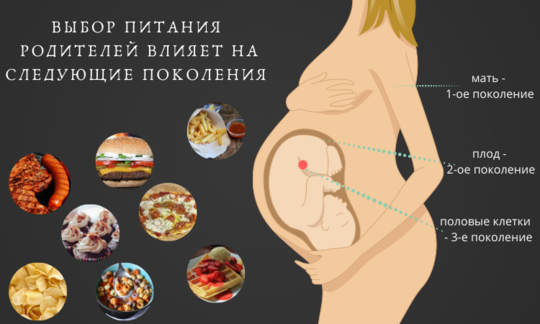
- среду, в которой человек развивался на стадии плода (например, доступ к питательным веществам, гормональный баланс и уровень стресса матери, плаценты).
- диету родителей.
Другими словами, вредные привычки влияют не только на тех, кто ими живет, но и на их детей.
В краткосрочной перспективе все эти изменения оказывают влияние на развитие детского мозга, рост, состав тела и обмен веществ. В долгосрочной перспективе они влияют на когнитивные способности ребенка, иммунитет и уровень энергии, влияя на школьные успехи, уровень образования, а также способность справляться с работой или даже общее состояние здоровья.5
В 1990 г. Баркер разработал парадигму «Истоки развития здоровья и болезней» (DOHaD) с той же самой идеей. В ней говорится, что условия до беременности, во время беременности и в период кормления грудью формируют развивающегося индивида. В случае неблагоприятной окружающей среды это приводит к подверженности определенным заболеваниям в зрелом возрасте (предрасположенности).1
2. Почему это происходит?
Уже на самых ранних стадиях развития (эмбриональная, стадии плода) организм может реагировать на экологические триггеры путем адаптации на клеточном, молекулярном и биохимическом уровнях. Если определенные стрессоры или раздражители, связанные с питанием, вызывают такие адаптации, то изменения в организме продолжаются и выполняются даже в отсутствие стимула, который их инициировал.6
Исследования на животных проводились по двум основным сценариям:
- Переедание матери - пища с высоким содержанием жира, высоким содержанием холестерина и высоким содержанием белка, которые приводят к материнскому ожирению .
- Недоедание матери - дефицит микроэлементов (например, Ca, Fe, Na, Zn) и макроэлементов (например, белка).
Если животные с низким весом при рождении получали высококалорийную диету, они, будучи взрослыми особями, имели тенденцию к увеличению накопления жира. Потому что в фазе плода организм был запрограммирован на ограничение затрат энергии как на адаптивный ответ на нехватку питания.7
Другое исследование6 показало, что диета с низким содержанием белка и ограничение калорий во время беременности приводят к изменениям в островках Лангерганса поджелудочной железы (например, уменьшению васкуляризации, снижению способности производить бета-клетки). Они также снижают чувствительность мышц к инсулину. Даже если после рождения и в детстве ребенок получает нормальное питание, изменения в органах необратимы и повышают предрасположенность к диабету или метаболическим заболеваниям.
Основными особенностями клеток, в период эмбриональной фазы и фазы плода, являются пластичность (способность клеток превращаться из одного вида в другой), а также развитие и структурирование органов. Поэтому воздействие любых факторов, способствующих заболеванию, в этот период сильнее, чем в более поздний период.
3. Метаболическое программирование
Программирование (метаболическое) питанием - это процесс, с помощью которого качество и количество питательных веществ, потреблённое во время беременности, оказывает длительное влияние на развитие плода.
Текущие исследования и эксперименты проводились только на животных (крысах и овцах). Их перекармливали или создавали дефицит определённых питательных веществ, чтобы увидеть, как это повлияет на их потомство. На людях были возможны только эпидемиологические исследования. Существует связь между условиями во время беременности и проблемами со здоровьем, которые развиваются у людей в более зрелом возрасте.
Почему с «программированием питания» не экспериментируют над людьми
«Метаболическое программирование» обычно происходит на эмбриональной стадии и стадии плода, когда клеточная пластичность наиболее высока. Чтобы изучить эмбриональные клетки и влияние, которое на них оказывает окружающая среда, ученым необходимо создать их, в первую очередь, путем экстракорпорального оплодотворения, что вызывает множество этических, моральных, религиозных и юридических проблем.
Большинство экспериментальных исследований на животных, в которых изменяются внешние условия и впоследствии исследуется воздействие на новорожденных и взрослых животных, не могут быть воспроизведены на людях.
Причины, по которым исследования на животных по-прежнему актуальны в этой области: 8
- крысы, мыши и люди имеют 99% схожих генов;
- их окружающей средой легко управлять;
- короткий жизненный цикл, и поэтому понятны изменения.
Качество и количество питательных веществ, потребляемых матерью во время беременности, могут привести к значительным изменениям в потомстве с точки зрения структуры мозга, почек и сердца. Это связано с повышенным риском ишемических заболеваний сердца и нарушений резистентности к инсулину.7
4. Что происходит на клеточном уровне?
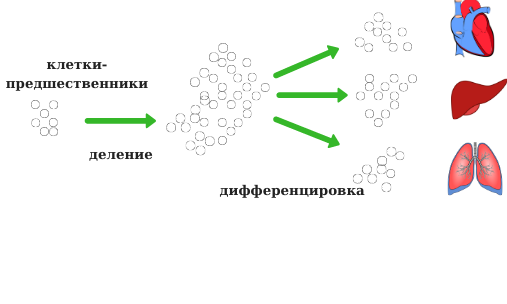
Развитие человека в матке основано на двух основных процессах: клеточном делении и клеточной дифференциации (специализации). Первоначально существует небольшой пул клеток (стволовых клеток), которые могут стать любым органом или тканью в организме. Эти клетки размножаются и после этого специализируются на свойствах особого органа. Время, в которое происходят эти процессы, различается в зависимости от органа. Сердце, например, формируется раньше, чем половые органы, а легкие развиваются только в последние недели беременности.
Изменения в рационе матери могут повлиять на процесс деления или дифференциации клеток. Нежелательные условия во время пролиферации (деления клеток) приводят, например, к органу меньшему по размеру, но с нормальными клеточными свойствами. Неблагоприятные условия при дифферениации, в свою очередь, могут привести к образованию органа нормального размера, но другой формы и с другой функциональностью.7
Результаты различных исследований показывают, что плохое питание матери во время беременности обычно приводит к изменениям в следующих областях:
- почки: у животных, испытывающих дефицит питательных веществ на стадии плода, почки на 30-40% меньше (производительность ??), чем обычно.7 Исследования на людях показывают, что австралийские аборигены на 20% чаще страдают от почечной недостаточности, чем представители европеоидной расы кавказкого населения.9
- мозг: исследования на крысах показывают, что недоедание снижает плотность капилляров в головном мозге и что плотность нейронов, отвечающих за регулирование аппетита, становится ниже.10
- поджелудочная железа: из-за уменьшения рациона питания, клетки поджелудочной железы животных имеют меньше островков Лангерганса, а кровоснабжение снижено.7
Является ли рост плода надежным показателем будущего здоровья ребенка?
До сих пор рост плода (вес и рост) был одной из наиболее исследуемых тем для установления взаимосвязи между условиями окружающей среды, развитием плода и состоянием здоровья в более позднем возрасте.
Исследования, опубликованные Баркером и его коллегами после наблюдения за тысячами людей, родившихся в течение двадцати лет, показали следующее: легкий вес при рождении считается прогнозом (предиктором) высокого кровяного давления, более высокого риска свертываемости крови, нарушения толерантности к глюкозе, риска диабета типа 2 и метаболического синдрома.7
Другие факторы, которые предсказывают будущие условия здоровья, включают в себя снижение окружности талии, большую окружность головы относительно длины тела и лёгкий вес по отношению к длине тела.
Исследование Розенбума11, посвященное голландскому голоду и его последствиям для детей, рождённых в этот период, ясно показывает, что недоедание во время беременности влияет на здоровье этих людей в более позднем возрасте.
С другой стороны, исследования на животных показывают, что это влияние условий окружающей среды выходит за рамки роста плода. Но поскольку это менее очевидно и выражается на разных уровнях, экспериментально наблюдать это сложно.
Даже если плод продолжает расти нормально, дефицит питательных веществ может оказать серьёзное влияние на будущее здоровье. С этой точки зрения вес при рождении не может быть единственным показателем здоровья во взрослой жизни.
Наблюдая за детьми, родившимися во время и после голландского голода, Розенбум пришел к выводу, что материнское недоедание во время беременности может в течение длительного времени влиять на здоровье человека, не влияя на размер ребенка при рождении10. Кроме того, последствия недоедания зависят от срока беременности и критического периода развития органов и систем.
Например, дети людей, забеременевших до голода в Голландии и испытывавшие недоедание на более поздних сроках беременности, подвергались повышенному риску инсулинорезистентности и нарушенной толерантности к глюкозе во взрослом возрасте. Те, кого зачали во время голода, подвергались повышенному риску высокого холестерина и ишемической болезни сердца в зрелом возрасте.11
Изменения в питании матери являются важными факторами влияния (предикторами), вызывающими изменения плода, а также самым сильным стимулом для «программирования плода». Однако есть много других факторов, которые одновременно влияют на пищевой статус плода: состав тела матери, возраст, физическая активность, приток крови к плаценте, эффективность переноса питательных веществ, гормональный баланс матери и т. д.
5. Эпигенетика - это основной процесс «программирования питанием»
Питание матери влияет на развивающийся плод через изменения в делении клеток и мх дифференциацию, а также на экспрессию генов плода (эпигенетические процессы).
Как работает эпигенетика
Подумайте о человеческом организме как об огромной сложной фабрике, в которой клетки тела являются основными рабочими единицами. Чтобы знать, как всё работает, клеткам нужна информация, основные правила и процессы. Эта огромная база данных правил и процессов находится в ДНК, тщательно записанной в виде информационных последовательностей, называемых генами. Существует более 20 000 генов, и каждая клетка имеет доступ к каждому из них, но не вся информация «считывается» и реализуется (воспроизводится). Информация выбирается и применяется в соответствии с дальнейшими инструкциями, так называемыми эпигенетическими маркерами. Все эти эпигенетические маркеры вместе образуют эпигеном, который уникален для каждого человека и находится под сильным влиянием окружающей среды. Подробнее о разнице между генетикой и эпигенетикой читайте здесь.
Эпигенетика (буквально "сверхгенетика") подобна выбору или определению отдельных частей этих правил и процессов. Они "активны", видны, и они командуют клетками, учитывать и экспрессироват эти части генома. Другие эпигенетические факторы отключают определённые гены и делают их недоступными, поэтому клетки не могут читать и использовать их информацию.
Основные механизмы эпигенетических модификаций
Основными механизмами, участвующими в эпигенетических модификациях, являются: 12
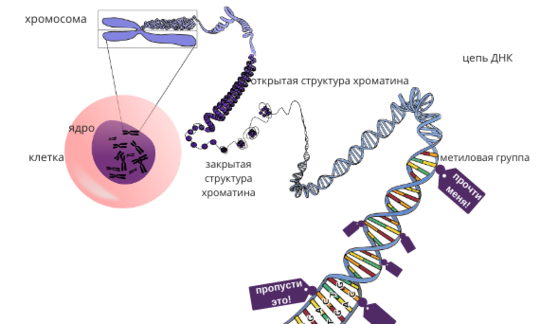
- Метилирование: метильная группа (функциональная группа в составе органических веществ), присоединённая к ДНК, которая изменяет функцию определенного гена.
- Модификация гистонов - чтобы соответствовать, длинная цепь ДНК должна быть обернута вокруг белковых структур, называемыми «гистонами». Таким образом формируется структура хроматина. Если гистон слишком плотно обёрнут белковыми структурами, клетка не сможет прочитать информацию в этой последовательности. Если связи между этими гистонами более свободные, информация считывается и применяется.
В одном эксперименте животным давали пищу, лишенную метильных групп, фолиевой кислоты, витамина B12 и метионина, в течение 8 недель до зачатия и в течение первых 6 дней беременности. Самцы этих овец были инсулинорезистентными и имели высокое кровяное давление.13
Это явление наиболее заметно у однояйцевых близнецов, которые живут в разных условиях. Даже если геном (вся наследственная информация) одинаков, у этих двух людей организм функционирует по разному и у них разное состояние здоровья.
Эпигенетика - хорошее и плохое
Роль эпигенетики заключается в том, чтобы помочь организму справиться с большими изменениями в окружающей среде и жизни. Например, она помогает организму выжить во время голода, изменяет женский организм во время беременности или организм подростков в период полового созревания.
Эпигенетические изменения наследуются
Важным фактом является то, что эти эпигенетические маркеры не фиксированы. Они на протяжении всей жизни могут меняться, например, под влиянием питания и окружающей среды. Некоторые из них даже могут быть унаследованы от предыдущих поколений и переданы дальше.
В эксперименте Центра репродуктивной биологии Университета штата Вашингтон беременные крысы подвергались воздействию относительно высоких уровней метоксихлора (инсектицида) и винклозолина (фунгицида). В результате у потомства мужского пола наблюдалось снижение выработки спермы и частое бесплодие. Исследование показало, что причиной этих проявлений стал процесс метилирования, затронувший два гена. Следующие четыре поколения наблюдались без применения каких-либо пестицидов. У 90% крыс-самцов были обнаружены такие же отрицательные эффекты.14
Исследования доктора Эрика Уотсона из Кембриджского университета показывают: если у бабушки по материнской линии или у дедушки по материнской линии есть конкретная генетическая мутация (известная как MTRR мутация), вызывающая дефицит фолиевой кислоты, то их генетически нормальные внуки, которые не наследуют генетическую мутацию, все еще подвержены риску определенных нарушений развития .16
7. Как ваш образ жизни может повлиять на здоровье ваших детей.
Долгое время ученые считали, что недоедание и западные болезни исключают друг друга. Удивительно, но эксперименты, в которых рацион питания беременных животных был ограничена, показали те же результаты на потомстве, что и эксперименты, в которых животные были перекормлены (например, высокое кровяное давление, непереносимость глюкозы, инсулинорезистентность и большая предрасположенность к ожирению). 17
Вот основные проявления последствий родительского питания, веса и образа жизни до и после зачатия на их потомстве:
| Питание и образ жизни родителей | Возможное влияние на детей |
| Жирная диета | Повышенное артериальное давление, сосудистые заболевания (эндотелиальная дисфункция) 18 |
| Белковая диета | Нарушения энергетического обмена, ожирение19 |
| Высокий уровень холестерина матери на ранней стадии беременности | Избыточный вес / ожирение, повышенное содержание жира в организме, повышенный уровень холестерина примерно с 4 лет 23 |
| Недоедание матери во время беременности | Повышенный синтез глюкозы в печени, нарушение окисления жирных кислот, резистентность к кетозу, нарушения усвоения глюкозы 2 |
| Переедание матери | Ожирение, непереносимость глюкозы, нарушенная регуляция аппетита мозгом |
| Низкобелковая диета | Нарушение эспрессии 102 генов в гипоталамусе и 36 генов в почках 20 |
| Ожирение у матери до и во время беременности и высокий уровень лептина (из-за ожирения) | Высокий уровень лептина во время развития гипоталамуса плода приводит к резистентности к лептину, гиперфагии и снижению способности ребенка регулировать аппетит. 21 Повышенное кровяное давление, большая склонность к ожирению и инсулинорезистентности 1 |
| Ожирение до беременности | Повышенный процент жировых отложений и повышенное систолическое кровяное давление у будущего ребенка 22 |
| Диета с низким содержанием железа матери до и во время беременности | Изменения в развитии сердца во время фазы плода, которые могут привести к повышению кровяного давления и нарушениям метаболизма жирных кислот 7 |
| Отец рано начал курить | Повышенный индекс массы тела у сыновей 23 |
| Употребление алкоголя отцом до зачатия | Низкая масса тела при рождении, задержка развития, нарушение иммунитета, поведенческие дефициты, гиперактивность и снижение работоспособности 24 |
Степень серьёзности этих эффектов связана с продолжительностью и количеством воздействия вредных веществ, а также периодом развития плода, в течение которого происходило вредное воздействие.
До недавнего времени ученые считали, что эпигенетические маркеры, влияющие на гены плода, оказывают длительное влияние на его здоровье и благополучие. Новые исследования исследоуют, остаются ли эти эпигенетические маркеры активными во взрослом возрасте. Это было бы хорошо, если бы условия окружающей среды изменялись в лучшую сторону.
Каждый человек несет ответственность за свои гены, Готфрид Шац
Другими словами, даже если определённые эпигенетические модификации имели место на стадии плода и привели к ухудшению здоровья, возможно изменить и обратить вспять их последствия во взрослом возрасте. Постоянное воздействие положительных факторов окружающей среды (например, здорового питания и образа жизни, положительных эмоций) может изменить активацию или деактивацию генов, предотвратить или обратить вспять хронические заболевания, такие как рак, диабет, высокое кровяное давление и проблемы с сердцем.
Большая часть этой информации всё ещё носит спекулятивный характер. Тем не менее, количество исследований эпигенетических модификаций и метаболического программирования постоянно растет. Другими словами, исследуется какое влияние на детей оказывает питание и образ жизни их родителей.
Литература
24 источников
- Tarrade A, Panchenko P, Junien C, Gabory A. Placental contribution to nutritional programming of health and diseases: epigenetics and sexual dimorphism. Journal of Experimental Biology 2015.
- Martínez JA, Cordero P, Campión J, Milagro FI. Interplay of early life nutritional programming on obesity, inflammation and epigenetic outcomes. Proc Nutr Soc. 2012 May;71(2):276-83.
- Wadhwa PD, Buss C, Entringer S, Swanson JM. Developmental Origins of Health and Disease: Brief History of the Approach and Current Focus on Epigenetic Mechanisms. Seminars in reproductive medicine. 2009;27(5):358-368. doi:10.1055/s-0029-1237424.
- Vickers, MV. Early Life Nutrition, Epigenetics and Programming of Later Life Disease. Nutrients 2014.
- Uauy R, Kain J, Corvalan C. How can the Developmental Origins of Health and Disease (DOHaD) hypothesis contribute to improving health in developing countries? The American journal of clinical nutrition. 2011.
- Patel MS, Srinivasan M. Metabolic Programming: Causes and Consequences. The Journal of Biological Chemistry, January 2011; 277.
- Langley-Evans SC. Nutritional programming of disease: unravelling the mechanism. Journal of Anatomy. 2009;215(1):36-51.
- Gunter C, Dhand R. Human biology by proxy. Nature 420, 509, 5 December 2002.
- Singh GR, Hoy WE. Kidney volume, blood pressure, and albuminuria: findings in an Australian aboriginal community. J Kidney Dis. 2004.
- Plagemann A, Harder T, Rake A, et all. Hypothalamic nuclei are malformed in weanling offspring of low protein malnourished rat dams. J Nutr. 2000.
- Roseboom TJ, van der Meulen JH, Ravelli AC, et all. Effects of prenatal exposure to the Dutch famine on adult disease in later life: an overview. Mol Cell Endocrinol. 2001.
- Kanherkar RR, Bhatia-Dey N, Csoka AB. Epigenetics across the human lifespan. Front Cell Dev Biol. 2014; 2: 49.
- Sinclair KD, Allegrucci C, Singh R, et al. DNA methylation, "insulinresistance", and blood pressure in offspring determined by maternal periconceptional B vitamin and methionine status. Proc Natl Acad Sci USA. 2007;104:19351–19356.
- Weinhold B. Epigenetics: The Science of Change. Environmental Health Perspectives. 2006.
- Anway MD1, Cupp AS, Uzumcu M, Skinner MK. Epigenetic transgenerational actions of endocrine disruptors and male fertility. Science. 2005 Jun 3;308(5727):1466-9.
- Padmanabhan N, Jia D, Geary-Joo C, Wu , Ferguson-Smith AC, Fung E. et all. Mutation in Folate Metabolism Causes Epigenetic Instability and Transgenerational Effects on Development. J. Cell, 2013 Sept. 2.
- Langley-Evans SC. Developmental programming of health and disease. Proc Nutr Soc. 2006.
- Khan IY, Taylor PD, Dekou V et all. Gender-linked hypertension in offspring of lard-fed pregnant rats. Hypertension. 2003.
- Daenzer M, Ortmann S, Klaus S, Metges CC. Prenatal high protein exposure decreases energy expenditure and increases adiposity in young rats. J Nutr. 2002.
- Langley-Evans SC, Bellinger L, McMullen S. Animal models of programming: early life influences on appetite and feeding behaviour. Matern Child Nutr. 2005.
- Samuelsson AM, Matthews PA, Argenton M, Christie MR, McConnell JM, Jansen EHJM et all. Diet-Induced Obesity in Female Mice Leads to Offspring Hyperphagia, Adiposity, Hypertension, and "InsulinResistance". A Novel Murine Model of Developmental Programming. Hypertension. 2008;51:383-392.
- Daraki V, Georgiou V, Chalkiadaki G, Karachaliou M, Koinaki S. Metabolic dysregulation in early pregnancy in association with offspring cardiometabolic risk in preschool children. Program of prevention and early diagnostic of obesity and neurodevelopment disorders in preschool age children, Crete, Greece, NSRF 2007-2013 project, MIS 349580.
- Pembrey ME, Bygren LO, Kaati G, Edvinsson S, Northstone K, Sjöström M, Golding J, ALSPAC Study Team. Sex-specific, male-line transgenerational responses in humans. Eur J Hum Genet. 2006 Feb; 14(2):159-66.
- Curley JP, Mashoodh R, Champagne FA. Epigenetics and the Origins of Paternal Effects. Hormones and behavior. 2011;59(3):306-314.


Комментарии