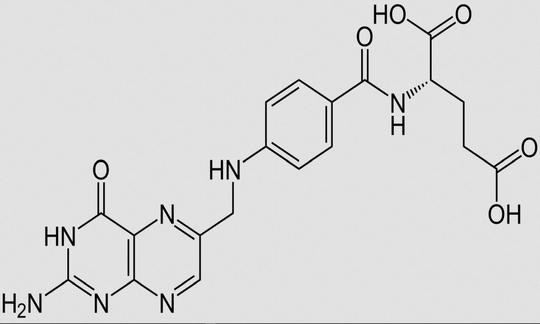
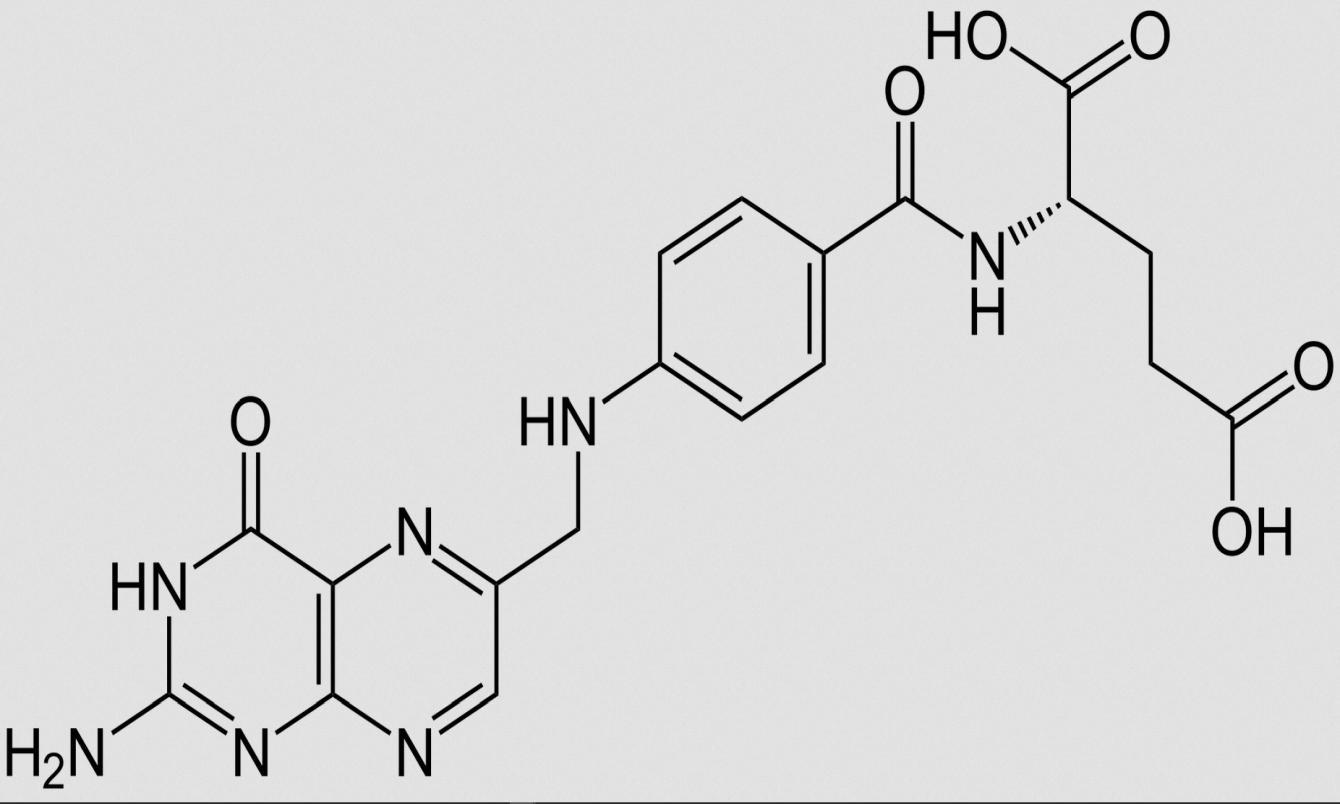
Folat als Folsäure-aktive Stoffgruppe (ex Vit. B9, B11)
Fazit:
Eine natürliche vegane Ernährung deckt den Bedarf an Folsäure ausserordentlich gut ab.
Nicht nur für Veganerinnern gilt, dass die ausreichende Zufuhr an Folsäure VOR einer Schwangerschaft für die gesunde Embryionalentwicklung wichtig ist.
Milch, Milchprodukte und (Muskel-) Fleisch enthalten praktisch kein Folat. Das gilt auch für Teigwaren und stark verarbeitete Produkte.
Nicht informierte Veganer begehen zu oft Ernährungsfehler. Darum ist dieser Link wichtig: Veganer essen oft ungesund. Vermeidbare Ernährungsfehler.
Vorkommen:
Wichtige pflanzliche Quellen von Folsäure sind Hülsenfrüchte, Kohlgemüse, grünes Blattgemüse und Getreideprodukte. Wichtige tierische Quellen sind Leber, Niere und Eier. Hohe Werte (µg Folat/100g) finden sich in:1,2
- Hülsenfrüchte: Mungobohnen (roh: 625; gekocht: 159), Kichererbsen (roh: 557; gekocht: 63), Linsen (roh: 479, gekocht: 181), Kidneybohnen (roh: 394; gekocht: 130), Bohnen weiss (roh: 388; gekocht: 102), Soja (Bohne roh: 375; Tofu: 22), Erdnüsse (roh: 240; geröstet: 97),
- Kohlgemüse: Grünkohl (141-212), Rosenkohl (61-179), Blumenkohl (57-125), Brokkoli (63-111),
- Grünes Blattgemüse: Spinat (frisch: 194, tiefgekühlt: 145), Petersilie (getrocknet: 180, frisch: 152), Feldsalat (145),
- Sonstiges: Backhefe (trocken: 2340; gepresst: 785), Grüne Minze (getrocknet: 530; frisch: 105), Basilikum (getrocknet: 310; frisch: 68), Weizenkeime (281), Quinoa (roh: 184, gekocht: 42), Hirse (roh: 85)
- Tierische Lebensmittel: Hühnerleber (roh: 588; gekocht: 578), Eier (47), Niere (41)
Lager- und Zubereitungsverluste:
Folate sind sauerstoffempfindlich, lichtempfindlich, wasserlöslich und hitzeempfindlich. Bereits bei der Lagerung (Sauerstoff, Licht) kommt es zu Veränderungen, die die Verwertbarkeit herabsetzen. Beim Kochprozess (Hitze, Löslichkeit) kommen weitere Verluste (10-70 %) hinzu. Die Zubereitungsverluste betragen bei Berücksichtigung, dass man folatreiche Lebensmittel häufig roh verzehrt, durchschnittlich 35 %. Polyglutamatformen sind stabiler (?) als die Monoglutamatform. Von den Derivaten sind THF und Methyl-THF die instabilsten.1,3
Ernährung / Gesundheit:
Tagesbedarf auf lange Sicht:
Wegen der Unterschiede von natürlichem Folat und reiner Folsäure bezüglich Verwertung führte man die Folat-Äquivalente ein. Dabei gilt: 1 µg Folatäquivalent = 1 µg Nahrungsfolat = 0.5 µg synthetische Folsäure.4 Um eine megaloplastische Anämie zu verhindern, muss man täglich mindestens 50 µg Folsäure (Pteroylmonoglutamat), das entspricht 100 µg Nahrungsfolat (Pteroylpolyglutamat) oder Folatäquivalente, zu sich nehmen. Um den Homocysteinspiegel unter 12 µmol/l halten zu können, braucht es eine tägliche Zufuhr von 200 µg Folatäquivalenten. Nach Sicherheitszuschlägen kommt man auf eine Zufuhrempfehlung von 300 µg für Erwachsene. Aufgrund des erhöhten Folatbedarfs in der Schwangerschaft (beschleunigte Zellvermehrung durch Vergrösserung / Entwicklung: Uterus, Plazenta, Brustgewebe, Blutvolumen, Fötus) empfiehlt man Schwangeren eine Zufuhr von 550 µg. Für Stillende empfiehlt man eine Zufuhr von 450 µg. Muttermilch enthält pro 100 ml ca. 8 µg Folat. Stillende geben pro Tag mit 750 ml Milch etwa 60 µg Folat ab.1
Mangelsymptome und Ursachen:
Man unterscheidet vier Stadien
- Abfall des Serumfolats bei normalen Körperspeicher
- Abfall des Folats in den Erythrozyten (<362 nmol/l): Man betrachtet mindestens 340 nmol/l als erwünschenswert, um den Homocysteinspiegel unter 12 µmol/l halten zu können.
- Beeinträchtigung der Erythropoese
- klinischer Folatmangel (hyperchrome makrozytäre Anämie, megaloblastischen Anämie): Nach vier Monaten folsäurefreier Ernährung kommt es zur Anämie. Die Blutbildung ist verlangsamt und die Zahl der roten Blutkörperchen reduziert. Diese sind aber nun überdurchschnittlich gross (makrozytär). Man spricht von Megaloblasten. Diese Veränderungen sind unabhängig davon, ob Folsäure- oder Vitamin B12-Mangel. Es treten Symptome auf:
- Zungenentzündung
- Entzündung der Lippenschleimhaut
- Malabsorption
- Sterilität bei beiden Geschlechter
- Neuropsychiatrische Schäden insbesondere bei älteren Menschen (Depression, Degeneration des Rückenmarks, Polyneuropathie)
- Missbildung des Föten (z.B. Neuralrohrdefekt) bzw. Abortus bei Schwangeren
Mangel an Folsäure ist weitaus häufiger die Ursache der megaloblastischen Anämie als ein Mangel an Vitamin B12. Ursachen sind vielfältig:7
- Zufuhrmangel: Einseitige Ernährung mit wenig Gemüse, wenig Vollkorn und einem hohen Anteil industriell verarbeiteter Produkte sind Ursachen für eine tiefe Zufuhr.
- Schnelles Wachstum von Gewebe: In der Schwangerschaft (häufige Schwangerschaften hintereinander, Schwangerschaften in oder gerade nach der Pubertät), in der Kindheit und bei Jugendlichen steigt der Bedarf an Folsäure erheblich.
- Medikamente: Zytostatika (wie Methotrexat hemmen Dihydrofolatreduktase) und Antibiotika (wie Sulfonamide) können den Folsäure-Status negativ beeinflussen.
- Rauchen
- Hoher Alkoholkonsum
- Chronische Krankheiten wie Schuppenflechte, Entzündungen, Krebs.
Überversorgung:
Über die Nahrungsaufnahme sind keine toxischen Wirkungen bekannt. Bei der Supplementierung ist Vorsicht geboten:1
- Wenn man bei Vitamin B12-Mangel mit Folsäure supplementiert, kann das die neurologischen Symptome des Vitamin B12-Mangels verschlimmern. Folsäure unterstützt die Zellneubildung. Diese braucht für die Proteinsynthese auch Methionin. Aufgrund des Vitamin B12-Mangels ist auch Methionin Mangelware. Methionin zieht weg vom Gehirn (wo es für die Methylierung von Myelin notwendig wäre) zur Proteinsynthese in die neuen Zellen.
- In Supplementen liegt die Folsäure vorwiegend in nicht metabolischer (unhydriert bzw. oxidiert) Monoglutamatform (PteGlu1) vor. Diese ist zwar fast vollständig resorbierbar, Enzyme (Dihydrofolatreduktase) müssen es aber noch metabolisieren (hydrieren bzw. reduzieren). Das kann die Enzyme (Dihydrofolatreduktase) an die Kapazitätsgrenze bringen. Folgen können eine Hemmung der natürlichen Killerzellaktivität sein.
- Hohe Folsäuregaben könnten zu einer Progression von Tumorzellen führen, wenn man sie nach deren Initiation verabreicht.
- Bei längerer Einnahme von 4 mg Folsäure pro Tag stellte man keine akuten Nebenwirkungen fest. Bei höheren Dosen kommt es zu Magen-Darm- und zu Schlafstörungen.
Funktionen im Körper etc.:1,3,7
- Zellwachstum: Folsäurehaltige Coenzyme spielen eine zentrale Rolle bei der Produktion von DNS beim Zellwachstum im ganzen Körper. Deshalb sind besonders Zellen, die schnell zerfallen und sich erneuern, wie Darmwand-, Lungen-, und Blutzellen, auf reichliche Versorgung mit Folsäure angewiesen. Folsäure fungiert meistens als Überträger sogenannter C1-Gruppen (C1-Bausteine). Das sind z.B. Methyl-, Formyl-, Methylen- und andere Gruppen. Wichtige C1-Quellen sind Serin, Glycin, Histidin und Formiat.
- Eiweiss-Stoffwechsel: Folsäurehaltige Coenzyme spielen eine zentrale Rolle in der Umwandlung von Aminosäuren und bei der Synthese von Struktur- und Funktionsproteinen. Dabei ist Folsäure in Form von C1-Überträgern beteiligt.
- Entwicklung des Fötus: Folsäure spielt eine entscheidende Rolle in der normalen Entwicklung des Fötus, besonders bei der Formung des Zentralnervensystems.
- Homocystein-Entgiftung und Methionin-Bildung: Homocystein entsteht beim Abbau der Aminosäure Methionin und wirkt toxisch auf Gehirn (neurologische Schäden) und Gefässe (Herzinfarkt, Schlaganfall). Folsäure und Vitamin B12 wandeln Homocystein in Methionin (wichtig für Myelinsynthese) zurück. Das geschieht wie folgt: Vitamin B12 überträgt die Methylgruppe (-CH3) von der Methyl-THF auf Homocystein. Es entsteht THF und Methionin. In dieser unmethylierten Form kann die Folsäure (THF) in die Zellen (z.B. Knochenmarkszellen) gelangen und ihre Wirkung (DNA-Synthese) ausüben.
- Cholin: Methyl-THF überträgt seine Methylgruppe auf Ethanolamin und wandelt es in Cholin um. Cholin ist unter anderem Bestandteil von Lecithin und ist notwendig für die Acetylcholinsynthese.
Aufnahme und Stoffwechsel:
Die Resorption findet im Zwölffinger- oder im Dünndarm statt.4 In unseren Lebensmitteln liegt Folsäure sowohl in Monoglutamat- als auch in Polyglutamatformen vor. Die Bioverfügbarkeit beträgt bei dem Monoglutamatformen über 90 % und bei den Polyglutamatformen nur etwa 20-50 %.5,4 In unserer Nahrung geht man von einer Gesamtverfügbarkeit von 40-50 % aus.1,5 Im Dünndarm enthaltene Enzyme (Konjugasen) spalten die Glutamatreste der Polyglutamatformen ab. Mit aktiven Transportmechanismen gelangt die Monoglutamatform in die Darmschleimhautzellen (Mukosazellen).6 Passive Diffusion ist bei hohen Dosen möglich.1 Der Transport im Blut erfolgt zum grössten Teil durch lockere Bindung an Plasmaproteine (Albumin, Transferrin etc.).6 In den Fäzes findet sich eine 5 bis 15-mal höhere Folsäureaktivität als in der zugeführten Nahrung. Dies ist auf eine mikrobielle Biosynthese in den unteren Darmabschnitten zurückzuführen. Einen Teil davon scheint der Körper zu verwerten. Denn bei längerer Therapie mit Sulfonamiden (ein Analoga der p-Aminobenzoesäure) kommt die Folsäureproduktion der Darmbakterien zum Erliegen und es kann zum Folatmangel kommen.1 Synthetisch hergestellte Folsäure in Monoglutamatform, welche man bei Nahrungsergänzungen und angereicherten Lebensmitteln einsetzt, nimmt der Körper zu nahezu 90 % auf.4
Speicherung, Verbrauch, Verluste:
Nach der Aufnahme über den Dünndarm erfolgt der Transport (in oxidierter Form) in die Leber, und dann nach Umwandlung (in die methylierte Form) in den Blutkreislauf. Zirkulierende Folate im Serum sind Monoglutamatformen (in der methylierten Form, v.a. 5-Methyl-H4Pte-Glu1). Vor der Aufnahme in die Zellen findet eine Demethylierung (Vitamin B12-abhängig) statt. Nach der Aufnahme in die Zellen erfolgt dann die Bildung von Polyglutamatformen. In dieser Form hält die Zelle die Folsäure fest. Der Transport wieder aus der Zelle benötigt eine vorangehende Hydrolyse zur Monoglutamatform. Enzyme, die für die Synthese und Hydrolyse von Polyglutamatformen verantwortlich sind, spielen eine bedeutende Rolle bei der Kontrolle der Folsäurespeicher. Der Gesamtspeicher im Körper (Leber, peripheres Gewebe) beträgt 5 bis 10 mg in Form nicht-methylierter Polyglutamate. 50 % davon befinden sich in der Leber.1 Einen wichtigen Faktor in der kurzfristigen Regulierung des Folathaushaltes stellt der enterohepatische Kreislauf dar. Da die Folatkonzentration in der Galle 10-fach höher ist als im Serum, kann der Körper durch dieses zirkulierende Folat die Schwankungen zwischen den Mahlzeiten ausgleichen. Hauptausscheidungsorgan ist die Niere, wo jedoch bei marginaler Versorgungslage durch effektive Rückresorption nur wenig Folat verloren geht.6
Strukturen:
Folsäure kommt in verschieden Formen vor:1
- Mono- und Polyglutamatformen: Man unterscheidet zwischen der Folsäureform (Pteroylmonoglutamat, PteGlu1), die ein Glutamat trägt, und den Folsäureformen (Pteroylpolyglutamate, PteGlu2-8), die zwischen 2 und 8 Glutamate tragen. Die beiden Varianten kommen in Lebensmitteln etwa im Verhältnis 1:1 (?) vor. In Nahrungsergänzungsmitteln setzt man die Monoglutamatform ein, da sie stabiler (?) und besser verfügbar ist. Im Körper ist die Transportform vorwiegend PteGlu1, die Speicherform vorwiegend PteGlu2-8.
- Reduzierte und oxidierte Formen: Die reduzierte und biologisch aktive Form der Folsäure ist Tetrahydrofolsäure (THF bzw. H4PteGlun). Die oxidierte Form von H4PteGlun ist die Dihydrofolsäure (H2PteGlun). Die oxidierte Form von H2PteGlun ist die Folsäure (PteGlun). Diese kommt weder im Körper noch in Lebensmitteln in nennenswerten Mengen vor. Pteroylmonoglutamat (PteGlu1) setzt man aber zur Vitaminisierung von Lebensmitteln und Nahrungsergänzungen ein.
- Verschiedene substituierte Formen: THF, Formyl-THF, Methyl-THF u.a. In frischen Nahrungsmitteln kommt vor allem Formyl-THF und Methyl-THF vor. Das Mischverhältnis schwankt je nach Lebensmittel:
- Obst und Gemüse: THF (10 %), Formyl-THF (25%), Methyl-THF (65 %)
- Hülsenfrüchte und Getreide: THF (3-8 %), Formyl-THF (38-48 %), Methyl-THF (14-20 %)
- Fleisch: THF (ca: 30 %), Formyl-THF (ca. 30 %), Methyl-THF (ca. 30 %)
- Milchprodukte: Formyl-THF (ca. 70 %)
Literatur / Quellen:
- Elmadfa I, Leitzmann C. Ernährung des Menschen. 5. Auflage. Eugen Ulmer: Stuttgart. 2015.
- USDA United Nations Department of Agriculture - Amerikanische Nährwertdatenbank.
- Elmadfa I, Meyer A. Ernährungslehre. 3. Auflage. Eugen Ulmer: Stuttgart. 2015.
- De Groot H, Farhadi J. Ernährungswissenschaft. 6. Auflage. Europa-Lehrmittel: Haan-Gruiten. 2015.
- Kasper H, Burghardt W. Ernährungsmedizin und Diätetik. 11. Auflage. Elsevier GmbH, Urban & Fischer Verlag: München. 2009.
- Biesalski HK, Grimm P. Taschenatlas der Ernährung;.3. Auflage. Georg Thieme: Stuttgart, New York. 2004.
- Zimmermann M, Schurgast H, Burgerstein UP. Burgersteins Handbuch Nährstoffe. 9. Auflage. Karl F. Haug Verlag: Heidelberg. 2000.
Der Bohnenschmortopf mit Tomaten und Salbei nach toskanischer Art gelingt leicht und ist gesund und sättigend.
Für diese weisse Bohnen mit Apfel, Birne und Bratkartoffeln weicht man davor Bohnen über Nacht in Wasser ein. Im Buch findet sich ein passender Löwenzahnsalat.
Dieses "Tailgate-Chili mit Borlotti-Bohnen" ist ein deftiges Gericht, das Sie nach Belieben einfach modifizieren können. Hier mit Maiskolben und Tomaten.
Vegetarische Gewürzpasten auf Basis von Hefeextrakt haben einen Umami-Geschmack. Man verwendet sie als Brotaufstrich oder Zutat in Suppen und Eintöpfen.
Bierhefe hat einen würzigen, leicht käseartigen Geschmack. Man verwendet sie deshalb zum Würzen oder als Käseersatz in Speisen. Argumente für Bio.
Backhefe (aktive Trockenhefe) setzt man zur Lockerung von Teigen ein (Backtriebmittel). Backhefe ist mit der Bierhefe verwandt. Bio-Qualität möglich.






Kommentare